Selektive Serotonin-Wiederaufnahmehemmer
- Autor(en): Peter Ritzmann
- Reviewer: Margrit Padrutt, Brigitte Woggon
- pharma-kritik-Jahrgang 18
, Nummer 5, PK412
Redaktionsschluss: 28. November 1996 - PDF-Download der Printversion dieser pharma-kritik Nummer
Übersicht
Die Antidepressiva aus der Gruppe der selektiven Serotonin-Wiederaufnahmehemmer («selective serotonin reuptake inhibitors» = SSRI) haben sich in der psychiatrischen wie auch in der hausärztlichen Praxis einen Platz erobert. Rechtfertigen die heutigen Erfahrungen aber einen Einsatz dieser teuren Medikamente generell als Mittel erster Wahl bei depressiven Erkrankungen, wie es uns die Herstellerfirmen glauben machen wollen?
Pharmakologie
Heute sind in der Schweiz fünf Antidepressiva auf dem Markt, welche als selektive Serotonin-Wiederaufnahmehemmer bezeichnet werden. Citalopram(1) (Seropram®), Fluoxetin(2) (Fluctine®), Fluvoxamin(3) (Floxyfral®), Paroxetin(4) (Deroxat®) und Sertralin(5) (Gladem®, Zoloft®) unterscheiden sich zwar in ihrer chemischen Struktur zum Teil erheblich voneinander, gleichen sich aber in ihren Wirkungen auf den menschlichen Organismus. Sie blockieren die Wiederaufnahme von Serotonin in die präsynaptische Nervenzelle, wodurch die Transmittersubstanz länger und in höherer Konzentration im synaptischen Spalt verbleibt. Diese Wirkung teilen die SSRI übrigens mit einem Teil der trizyklischen Antidepressiva wie z.B. Clomipramin (Anafranil®). Im Gegensatz zu den tri- und tetrazyklischen Antidepressiva beeinflussen sie aber die Wiederaufnahme von Noradrenalin kaum. Ausserdem zeigen sie in vitro weniger Affinität zu postsynaptischen adrenergen, cholinergen, histaminergen und dopaminergen Rezeptoren.
In ihrem pharmakodynamischen Verhalten unterscheiden sich die SSRI nur wenig voneinander. Einige in vitro feststellbare Unterschiede sind wahrscheinlich klinisch nicht bedeutsam.
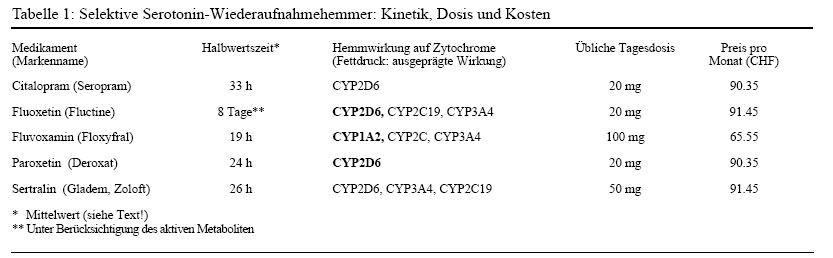
Wichtiger sind die Unterschiede im pharmakokinetischen Verhalten, vgl. Tabelle 1. Nur Fluoxetin hat einen aktiven Metaboliten (Norfluoxetin), der von grösserer praktischer Bedeutung ist. Fluoxetin zeichnet sich durch eine besonders langanhaltende Wirkung aus: bei einmaliger täglicher Verabreichung kumuliert es stärker als die anderen SSRI und wird nach Absetzen noch über mehrere Wochen aus dem Körper ausgeschieden.(6) Für alle SSRI ist aber zu beachten, dass der Metabolismus (wie bei den trizyklischen Antidepressiva) sehr grosse interindividuelle Unterschiede aufweist. Die einzelnen SSRI beeinflussen sodann das Zytochrom-P450-System in recht unterschiedlicher Weise, siehe unten (Interaktionen).
Klinische Wirksamkeit bei Depression
Dass die selektiven Serotonin-Wiederaufnahmehemmer in der Behandlung depressiver Störungen wirksamer als Placebo sind, ist unbestritten. Dies gilt sowohl für die kurzzeitige wie für die längerfristige Anwendung. Klinische Studien, in welchen die kurzzeitige Wirksamkeit (meistens 6 Wochen) von SSRI mit anderen Antidepressiva verglichen wurde, sind in grosser Zahl publiziert worden. Viele dieser Studien sind aber relativ klein und deshalb in ihrer Aussagekraft beschränkt. In den letzten Jahren wurden deshalb mehrere Meta-Analysen von doppelblinden SSRI-Vergleichsstudien veröffentlicht. Die in den Studien verwendeten Depressions-Skalen (meistens «Hamilton Depression Rating Scale») dienten als Vergleichsbasis. Als Effektgrösse wurde die mittlere Veränderung der in den Depressions-Skalen erreichten Punktezahl gewählt. Eine erste, 1992 publizierte Arbeit verwendete nur Vergleichsstudien mit Imipramin (Tofranil®) und Amitriptylin (Saroten®, Tryptizol®), bei welchen alle für die Meta-Analyse benötigten Daten veröffentlicht waren. Trizyklische Antidepressiva und SSRI zeigten eine vergleichbare antidepressive Wirksamkeit. (7)
Bei einer häufig zitierten britischen Meta-Analyse, welche 1993 veröffentlicht wurde, wurden erheblich mehr Studien mit eingeschlossen, nämlich alle, welche ein SSRI mit einem «trizyklischen oder verwandten Antidepressivum» verglichen. So konnten die Ergebnisse von insgesamt 49 doppelblinden Vergleichsstudien gepoolt werden. Dabei resultierte ein minimaler (nicht-signifikanter) Vorteil der Vergleichssubstanzen gegenüber den SSRI als Gruppe. 14 Studien wurden von der Analyse ausgeschlossen, weil sie keine vergleichbaren Depressions-Skalen verwendeten.(8)
Eine neuere, ebenfalls britische Meta-Analyse konnte auf die Daten von 55 randomisierten, doppelblinden Studien bei gut 4600 Personen zurückgreifen. Hier wurden nur Vergleichsstudien mit trizyklischen Antidepressiva oder Maprotilin (Ludiomil®) zur Analyse verwendet. Um eine Verfälschung zugunsten der SSRI zu vermeiden, musste bei den verwendeten Studien die durchschnittliche Tagesdosis der trizyklischen Antidepressiva mindestens 100 mg betragen. Alle Studien verwendeten als Aufnahmekriterium eine schwere depressive Störung gemäss DSM III-R oder entsprechende Kriterien. Insgesamt fand sich kein Unterschied in der Wirksamkeit zwischen den SSRI und den Trizyklika. Auch wenn die SSRI einzeln analysiert wurden, waren die Unterschiede gegenüber den Trizyklika nicht signifikant. Während sich für Fluoxetin, Paroxetin und Fluvoxamin diese Analyse auf relativ viele Daten stützt (1693, 1176 bzw. 996 Behandelte) konnten für Sertralin und Citalopram nur relativ wenige Studien gepoolt werden (495 bzw. 270 Behandelte).
Wenn verschiedene Untergruppen verglichen wurden, waren die SSRI bei hospitalisierten Personen und bei Personen mit durchschnittlich höheren Depressions-Scores etwas weniger wirksam als die Trizyklika. Die Unterschiede waren in beiden Untergruppen grenzwertig signifikant. Ebenfalls signifikante Unterschiede fanden sich, wenn die Studien entsprechend den verwendeten Kontroll-Antidepressiva in zwei Gruppen unterteilt wurden. Dabei erschien die Wirksamkeit von trizyklischen Antidepressiva mit deutlicher Wirkung auf die Serotonin-Wiederaufnahme (Clomipramin, Amitriptylin) derjenigen der SSRI insgesamt leicht überlegen. Die übrigen Trizyklika (welche vorwiegend die Noradrenalin-Wiederaufnahme hemmen) waren ihrerseits den SSRI leicht unterlegen. (9)
Kritik der vorliegenden «Evidenz»
Eine insgesamt vergleichbare Wirksamkeit von SSRI und trizyklischen Antidepressiva erscheint somit heute gut belegt. Einige Schönheitsfehler schmälern allerdings die Freude an diesem «Beweis»: Sind die veröffentlichten (und damit für die Meta-Analyse zugänglichen) Studien repräsentativ für alle durchgeführten Studien? Wenn günstige Resultate eher veröffentlicht werden als ungünstige, so wird das Resultat einer Meta-Analyse in die «günstige» Richtung verfälscht («publication bias»).
Sind die Studien von ihrer Anlage her überhaupt in der Lage, relevante Unterschiede aufzudecken? Die Studienpopulationen sind recht heterogen, z.B. bezüglich der Dauer der depressiven Störungen. Bei Depressionen, die erst seit kurzer Zeit bestehen, könnte eine hohe Spontanheilungsrate einen Wirksamkeitsunterschied verbergen. Von den Personen mit länger vorbestehenden Störungen ist dagegen anzunehmen, dass sie mindestens zum Teil schon zuvor erfolglos mit trizyklischen Antidepressiva behandelt wurden. Dies könnte zu einer Verfälschung der Resultate zugunsten der SSRI führen.(8)
Zu bemerken ist auch, dass sich Personen, welche Hilfe in einer Praxis suchen, wahrscheinlich erheblich von Leuten unterscheiden, die sich (wie in den USA häufig) auf die Werbung für eine klinische Studie melden. Es ist denkbar, dass solche «Freiwillige» die Behandlung vergleichsweise häufiger bei relativ «gutartigen» Nebenwirkungen (z.B. Mundtrockenheit) abbrechen. Jedenfalls scheinen die Aussteigerraten in nordamerikanischen Studien erheblich höher zu sein als in europäischen.(10)
Vergleiche zwischen verschiedenen selektiven Serotonin-Wiederaufnahmehemmern
Klinische Vergleichsstudien zwischen den einzelnen SSRI sind bisher nicht viele veröffentlicht worden. In ihrer antidepressiven Wirksamkeit unterschieden sich die Substanzen offenbar nicht wesentlich. Am häufigsten wurden wohl Vergleiche mit Fluoxetin durchgeführt. Dabei wurde festgestellt, dass die Wirkung anderer SSRI zum Teil etwas früher eintritt als diejenige von Fluoxetin (signifikante Unterschiede in der Wirksamkeit nach drei Wochen).(11,12)
Andere psychiatrische Indikationen
Serotonin-Wiederaufnahmehemmer sind möglicherweise noch bei verschiedenen anderen Indikationen nützlich.
Recht gut dokumentiert ist ihre Wirksamkeit bei Zwangsstörungen. Fluoxetin, Fluvoxamin und Sertralin waren in kontrollierten Studien wirksamer als Placebo. Die drei grössten dieser Placebo-kontrollierten Studien wurden in einer Meta-Analyse einer entsprechenden Arbeit mit Clomipramin (Anafranil®) gegenübergestellt. Clomipramin gilt als das am besten dokumentierte Medikament bei Zwangsstörungen. Die als vergleichbare Effektgrösse berechnete Wirkung (Verbesserung unter Behandlung abzüglich Placebowirkung, gewichtet nach Studiengrösse) war aber bei Clomipramin signifikant höher als bei den drei SSRI. Unter Clomipramin war auch der Anteil der klinisch stark gebesserten Personen signifikant höher und die Aussteigerrate insgesamt signifikant kleiner.(13)
Placebokontrollierte Doppelblindstudien mit Fluvoxamin und Paroxetin belegen auch eine gewisse Wirksamkeit bei Panikstörungen. Aufgrund von Untersuchungen mit Clomipramin wird vermutet, dass SSRI bei dieser Indikation wirksamer sein könnten als andere Antidepressiva.(14)
Der Einsatz bei anderen Angststörungen und bei Alkoholmissbrauch ist im Vergleich dazu noch spärlicher dokumentiert. Grösser waren zwei Studien bei Personen mit Bulimie. Die Symptome der Ess-/Brechsucht wurden von Fluoxetin signifikant besser beeinflusst als von Placebo.(15)
Nicht-psychiatrische Indikationen
Eine Wirksamkeit der SSRI bei chronischen Schmerzen konnte bisher nicht nachgewiesen werden. In einer kontrollierten Studie bei Personen mit neuropathischen Schmerzen war Fluoxetin so wenig wirksam wie Placebo und war Desipramin und Amitriptylin unterlegen. Dagegen war Fluoxetin (als Dauertherapie) wirksamer als Placebo bei der Behandlung des prämenstruellen Syndroms. (12) In der Behandlung von unkontrolliertem Schreien nach zerebrovaskulären Insulten war Citalopram wirksamer als Placebo. (16) Bei übergewichtigen Personen führte Fluoxetin in höheren Dosen zu statistisch signifikanten Gewichtsreduktionen.(16)
Unerwünschte Wirkungen
Die SSRI verursachen andere unerwünschte Wirkungen als die trizyklischen Antidepressiva. In klinischen Studien wurden gastrointestinale Störungen (Brechreiz/Erbrechen, Durchfall) und Kopfschmerzen am häufigsten beobachtet. Häufiger als die Vergleichssubstanzen verursachen die SSRI ausserdem Einschlafstörungen, Unruhe und Angst sowie Gewichtsabnahme und sexuelle Störungen (insbesondere eine Verzögerung der Ejakulation sowie verminderte Libido). Seltener als unter den trizyklischen Antidepressiva werden hingegen ein trockener Mund, Verstopfung, Sehstörungen, Schwindel und Sedation wie auch kardiovaskuläre Symptome (Herzklopfen, orthostatische Hypotonie u.a.) beobachtet. Die SSRI beeinflussen die elektrische Erregungsleitung am Herzen weniger als die trizyklischen Substanzen. Dies dürfte der wichtigste Grund dafür sein, dass Intoxikationen mit SSRI anscheinend seltener zum Tod führen. (6,17) Es sind aber auch Todesfälle infolge von SSRI-Vergiftungen bekannt!
Die vor einigen Jahren diskutierte Frage, ob Fluoxetin mehr als andere Antidepressiva suizidale Tendenzen verstärken könne, kann aufgrund der heute vorliegenden Daten verneint werden. Seltenere, aber eventuell klinisch relevante Störungen im Zusammenhang mit der Einnahme von SSRI sind allergische Hautausschläge, inadäquate ADH-Ausschüttung (SIADH), extrapyramidale Bewegungsstörungen und Entzugssymptome. Letztere scheinen besonders unter Paroxetin, seltener auch unter Sertralin aufzutreten.(6,18)
Die meisten Berichte über unerwünschte Wirkungen betreffen Fluoxetin. Dies ist aber vermutlich vor allem darauf zurückzuführen, dass diese Substanz über Jahre hinweg alleiniger Vertreter der SSRI auf dem amerikanischen Markt war. Ob die neueren Substanzen, welche eine geringere Tendenz zur Akkumulation im Körper aufweisen, deshalb auch besser verträglich wären, erscheint aus heutiger Sicht eher unwahrscheinlich.
Verträglichkeit: Therapieabbrüche
Interessanter als die Unterschiede im Nebenwirkungsprofil gegenüber den trizyklischen Antidepressiva ist die Frage, ob und in welchem Ausmass dadurch die Verträglichkeit insgesamt verbessert wird. Wenn man dafür die Zahl der Therapieabbrüche als Mass nimmt, muss allerdings berücksichtigt werden, dass Therapieabbrüche auch in klinischen Studien nicht einheitlich geregelt werden und einen grossen Ermessensspielraum seitens der Untersucher zulassen. So waren beispielsweise in europäischen Fluoxetin-Studien allgemein Therapieabbrüche wesentlich seltener als in amerikanischen Studien. Infolge dieses Unterschiedes ergab sich auch nur in den amerikanischen (nicht jedoch in den europäischen) Studien ein signifikanter Verträglichkeitsvorteil von Fluoxetin.(10) Es ist verständlich, dass die Herstellerfirma sich in erster Linie auf die für ihr Präparat vorteilhaften amerikanischen Daten stützt.(17)
Ein signifikanter Vorteil der SSRI gegenüber den Trizyklika fand sich aber auch in einer Meta-Analyse, welche Vergleichsstudien zwischen allen fünf SSRI mit Trizyklika einschloss (4481 Behandlungen): unter SSRI kam es in 15% zu Therapieabbrüchen wegen unerwünschten Wirkungen, unter Trizyklika dagegen in 19% (p<<0,01). Therapieabbrüche, die mangels klinischem Erfolg vorgenommen wurden, waren dagegen mit den beiden Medikamentengruppen sehr ähnlich.(19)
In einer der oben zitierten Meta-Analysen wurde ebenfalls neben der Wirksamkeit auch die Zahl der Therapieabbrüche untersucht. Hier unterschieden sich die SSRI kaum von den Vergleichssubstanzen, unter welchen sich allerdings auch nicht-trizyklische Substanzen befanden. Weder die Therapieabbrüche insgesamt, die Abbrüche wegen unerwünschten Wirkungen noch diejenigen wegen ungenügender Wirksamkeit waren für SSRI und Vergleichssubstanzen signifikant verschieden.(8)
Diese widersprüchlichen Ergebnisse lassen vermuten, dass die Trizyklika mit ihren anticholinergen Eigenschaften häufiger bemerkbare Nebenwirkungen verursachen. Ob diese nun toleriert werden oder eine Behandlung verunmöglichen, hängt wohl wesentlich von der Motivation der Behandelten und der Behandelnden ab. Somit ist die praktische Relevanz der etwas besseren Verträglichkeit der SSRI schwierig abzuschätzen.
Anwendung bei Älteren oder körperlich Kranken
Ältere und kranke Menschen tolerieren Sedation und kardiovaskuläre Nebenwirkungen der Trizyklika oft besonders schlecht. Diesen Personen bringt das andersartige Nebenwirkungsprofil der SSRI vermutlich mehr Gewinn als Jungen und körperlich Gesunden.
Gemäss einigen Studien, in denen SSRI bei älteren Menschen angewendet wurden, sind Wirksamkeit und Verträglichkeit im Alter nicht anders als bei jungen Leuten. In den meisten Studien wurden allerdings Personen mit begleitenden Erkrankungen ausgeschlossen. (20)
Trizyklische Antidepressiva gleichen in ihren kardialen Auswirkungen den Antiarrhythmika der Klasse I, welche in der grossen CAST-Studie zu einer erhöhten Sterblichkeit bei koronarer Herzkrankheit geführt hatten. Von der Verabreichung von trizyklischen Antidepressiva an Herzkranke wird deshalb heute abgeraten. Da die SSRI das periphere adrenerge System wie auch das Herz-Erregungsleitsystem weniger beeinflussen, erscheinen sie grundsätzlich als die bessere Option bei Herzkranken. Leider ist die Anwendung von SSRI bei vorbestehenden Herz-/Kreislauferkrankungen bisher aber kaum dokumentiert. Ob sie eine sicherere Alternative darstellen, ist deshalb noch zu beweisen.(21) Zumindest bei Überdosierung scheinen auch SSRI Rhythmusstörungen verursachen zu können.
Interaktionen
Die SSRI verursachen andere Interaktionen als die trizyklischen Substanzen. Von besonderer Bedeutung ist die Hemmwirkung auf verschiedene Zytochrom-P450-Isoenzyme. Nach heutigem Wissen weist jedes der SSRI ein individuelles Hemmspektrum auf, jedoch ist in allen Fällen wenigstens eines der Zytochrome betroffen. In der Tabelle 1 sind die von den verschiedenen Medikamenten gehemmten Isoenzyme – soweit bekannt – bezeichnet. Die meisten SSRI können z.B. bei gleichzeitiger Verabreichung mit trizyklischen Antidepressiva zu einem Anstieg der Trizyklika-Plasmaspiegel führen. Auch andere psychotrope Medikamente (Benzodiazepine, Neuroleptika) werden eventuell beeinflusst. SSRI, die das Zytochrom CYP3A hemmen, können mit Terfenadin (Teldane®) zusammen zu Herzrhythmusstörungen führen. Gesamthaft scheint das Risiko von klinisch relevanten Interaktionen für Citalopram und Sertralin etwas geringer zu sein.
Bei allen SSRI ist jedoch das Risiko von schweren Allgemeinreaktionen bei Kombination mit Monoaminoxidase-Hemmern («Serotonin-Syndrom») zu beachten. Möglicherweise wird bei gleichzeitiger Anwendung auch die Toxizität von Lithium verstärkt. Da die SSRI nach Absetzen noch unterschiedlich lange in relevanten Konzentrationen im Körper verbleiben, soll eine Behandlung mit einem MAO-Hemmer frühestens zwei Wochen (bei Fluoxetin: fünf Wochen) später begonnen werden.(6)
Dosierung und Kosten
Die SSRI werden üblicherweise einmal täglich verabreicht. Eine Ausnahme ist Fluvoxamin, das bei höherer Dosierung (über 100 mg/Tag) auf zwei Einzeldosen aufgeteilt werden soll. Die heute üblichen Tagesdosen sind in der Tabelle 1 zu finden.
Die SSRI sind teure Medikamente. Trizyklische und ähnliche Antidepressiva kosten zwischen 20 und 50 Franken pro Monat, d.h. bis zu viermal weniger als die meisten SSRI. Es ist zwar denkbar, dass die Wahl eines SSRI die Behandlungskosten auch günstig beeinflussen kann, z.B. indem andere Kosten (Anzahl Konsultationen, Laboruntersuchungen u.a.) gesenkt würden. Um solche Effekte abschätzen zu können, wären prospektive kontrollierte Untersuchungen vonnöten, welche bis heute nicht vorliegen.
Schlussfolgerungen
Die selektiven Serotonin-Wiederaufnahmehemmer haben sich auf dem grossen Markt für Antidepressiva einen wichtigen Platz erobert. Neben dem Nimbus des Neueren und deshalb Besseren sind es sicher auch eine einfachere Dosierung und die seltener auftretenden anticholinergen Nebenwirkungen, welche zur Attraktivität dieser Medikamente in der Praxis beitragen.
Gemessen an den Ansprüchen einer «Evidence Based Medicine» relativieren sich ihre Vorteile gegenüber älteren Antidepressiva allerdings beträchtlich. Die Wirksamkeit der SSRI bei depressiven Störungen liegt im Bereich derjenigen der trizyklischen Antidepressiva. Als wirklich gesichert kann hingegen nur gelten, dass sie im Durchschnitt nicht besser wirken. Schwere Verlaufsformen (melancholische Depressionen) scheinen weniger anzusprechen, bei hospitalisierten Personen ist ihre Anwendung (mit Ausnahme von Fluvoxamin) noch zu wenig dokumentiert. Gut dokumentiert ist dagegen ihre geringere Gefährlichkeit bei Intoxikationen und dass sie weniger unangenehme Nebenwirkungen verursachen. Anderseits muss auch das (individuell unterschiedliche) Interaktionsrisiko beachtet werden. Ob die Vorteile der SSRI die höheren Medikamentenkosten zu rechtfertigen vermögen, kann nicht generell entschieden werden. Gelegentlich mögen körperliche Erkrankungen die Medikamentenwahl mitbestimmen. Immer muss die Entscheidung für oder gegen ein SSRI aber sorgfältig individuell getroffen werden.
Noch schwieriger ist es, klare Vorteile eines einzelnen Serotonin-Wiederaufnahmehemmers zu erkennen. Die vorhandenen Unterschiede im pharmakokinetischen Verhalten lassen sich kaum eindeutig für die eine oder andere Substanz verwenden. Fluoxetin ist bisher die Substanz, die in ihrer Anwendung weitaus am besten dokumentiert ist. Fluvoxamin zeichnet sich dagegen durch einen deutlich günstigeren Preis aus.
Kommentare
Gesamthaft dürfte die antidepressive Wirkung der SSRI bestenfalls jener der trizyklischen Antidepressiva gleichkommen. Letztere verursachen zweifellos mehr kardiale Probleme und auch nicht selten eine Gewichtszunahme. Anderseits haben auch die SSRI etliche störende Nebenwirkungen. Letztere sind zwar medizinisch weniger gravierend, aber dennoch geeignet, die Compliance zu erschweren.
Auf Grund besserer Verträglichkeit können SSRI bei manchen therapieresistenten Patienten viel höher dosiert werden als Trizyklika und Maprotilin. Dadurch ist es möglich, auch Patienten mit echter Therapieresistenz wirksam zu helfen. Als Hilfsmittel bietet sich die Bestimmung der Plasmaspiegel an.
Literatur
- 1) Beutler M. pharma-kritik 1991; 13: 7-8
- 2) Beutler M. pharma-kritik 1991; 13: 74-6
- 3) Häberli T. pharma-kritik 1984; 6: 57-9
- 4) Kappeler T. pharma-kritik 1994; 16: 9-11
- 5) Majstorovic R. pharma-kritik 1994; 16: 73-4
- 6) Rudorfer MV et al. Drug Saf 1994; 10: 18-46
- 7) Kasper S et al. Drugs 1992; 43 (Suppl. 2): 11-23
- 8) Song F et al. Br Med J 1993; 306: 683-7
- 9) Anderson IM, Tomenson BM. J Psychopharmacol 1994; 8: 238-49
- 10) Gram LF. N Engl J Med 1994; 331: 1354-61
- 11) Lane R et al. J Psychopharmacol 1995; 9 (Suppl): 163-78
- 12) Finley PR. Ann Pharmacother 1994; 28: 1359-69
- 13) Greist JH et al. Arch Gen Psychiatry 1995; 52: 53-60
- 14) Johnson MR et al. Drugs 1995; 49: 328-44
- 15) Wood A. Int Clin Psychopharmacol 1993; 8: 295-9
- 16) Andersen G. Drugs Aging 1995; 6: 105-11
- 17) Pande AC, Sayler ME. Int Clin Psychopharmacol 1993; 8: 2647-9
- 18) Kappeler T. pharma-kritik 1995; 17: 69-70
- 19) Montgomery SA et al. Int Clin Psychopharmacol 1993; 9: 47-53
- 20) Harris MG, Benfield P. Drugs Aging 1995; 6: 64-84
- 21) Roose SP, Glassman AH. J Clin Psychiatry 1994; 55 (Suppl A): 83-7
Standpunkte und Meinungen
- Es gibt zu diesem Artikel keine Leserkommentare.
Copyright © 2024 Infomed-Verlags-AG
PK412
Gratisbuch bei einem Neuabo!
pharma-kritik abonnieren
-
Jahrgang 45 / 2023
Jahrgang 44 / 2022
Jahrgang 43 / 2021
Jahrgang 42 / 2020
Jahrgang 41 / 2019
Jahrgang 40 / 2018
Jahrgang 39 / 2017
Jahrgang 38 / 2016
Jahrgang 37 / 2015
Jahrgang 36 / 2014
Jahrgang 35 / 2013
Jahrgang 34 / 2012
Jahrgang 33 / 2011
Jahrgang 32 / 2010
Jahrgang 31 / 2009
Jahrgang 30 / 2008
Jahrgang 29 / 2007
Jahrgang 28 / 2006
Jahrgang 27 / 2005
Jahrgang 26 / 2004
Jahrgang 25 / 2003
Jahrgang 24 / 2002
Jahrgang 23 / 2001
Jahrgang 22 / 2000
Jahrgang 21 / 1999
Jahrgang 20 / 1998
Jahrgang 19 / 1997
Jahrgang 18 / 1996
Jahrgang 17 / 1995
Jahrgang 16 / 1994
Jahrgang 15 / 1993
Jahrgang 14 / 1992
Jahrgang 13 / 1991
Jahrgang 12 / 1990
Jahrgang 11 / 1989
Jahrgang 10 / 1988
Kennen Sie "100 wichtige Medikamente" schon?
Die Liste der 100 Medikamente sehen Sie auf der Startseite von 100 Medikamente.