ACE-Hemmer nach Herzinfarkt
- Autor(en): Alex Flückiger
- Reviewer: Walter Angehrn, Osmund Bertel, Augusto F. Gallino
- pharma-kritik-Jahrgang 17
, Nummer 15, PK442
Redaktionsschluss: 30. April 1996 - PDF-Download der Printversion dieser pharma-kritik Nummer
Übersicht
Die linksventrikuläre Auswurffraktion hat sich als wichtigster prognostischer Faktor nach Herzinfarkt erwiesen. Beträgt sie weniger als 30%, so ist die Einjahres-Mortalität fünfmal höher als bei normaler Funktion des linken Ventrikels.(1) Auch wenn im akuten Stadium eines Myokardinfarkts keine Herzinsuffizienz manifest wird, kann sich im Verlauf von Wochen bis Monaten eine progrediente Dilatation und Dysfunktion des linken Ventrikels entwickeln.(2) Dabei spielen neurohumorale Reaktionen eine zentrale Rolle: Die Aktivierung des sympathisch-adrenergen und des Renin-Angiotensin-Systems hat eine Steigerung der Vor- und Nachlast zur Folge, welche ihrerseits die Wandspannung des linken Ventrikels erhöht. Gleichzeitig kommt es unter dem Einfluss von Angiotensin II häufig zu einer Hypertrophie nicht-infarzierter Myokardbezirke. Diese Vorgänge werden als Teil des «Remodeling» hauptsächlich nach grösseren Infarkten beobachtet.
ACE-Hemmer haben einen festen Platz in der Behandlung aller Stadien einer chronischen Herzinsuffizienz, seitdem ihr vitaler Nutzen bei einer grossen Patientenzahl dokumentiert worden ist.(3,4) Gegenüber anderen Vasodilatatoren haben sie grundsätzlich den Vorteil, die Vor- und Nachlast zu senken, ohne Gegenregulationsmechanismen auszulösen. Bei langfristiger Anwendung wirken ACE- Hemmer einer progredienten linksventrikulären Dilatation und Dysfunktion entgegen.(5)
Nach einem Herzinfarkt können sich verschiedene Eigenschaften der ACE-Hemmer als vorteilhaft erweisen; mögliche Wirkungsmechanismen sind in der Tabelle 1 zusammengestellt.
In den letzten Jahren sind mehrere Studien der Frage nachgegangen, ob ACE-Hemmer die Prognose verbessern, wenn sie bereits im akuten bis subakuten Stadium eines Myokardinfarktes eingesetzt werden, und ob auch Infarktpatienten ohne manifeste Herzinsuffizienz von einer solchen Behandlung profitieren.
Klinische Studien
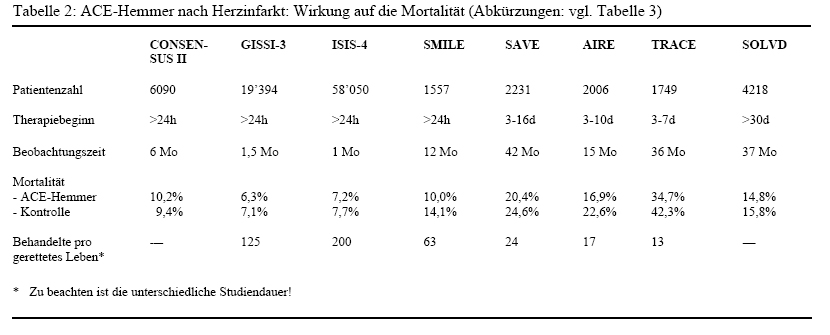
Bisher sind die Ergebnisse von acht grossen, unterschiedlich konzipierten Studien publiziert worden, welche die Mortalitäts-Senkung als Erfolgsparameter gewählt haben (siehe Tabelle 2).
Akutes Infarktstadium / Verwendung eines ACE-Hemmers bei allen Patienten
Die doppelblind durchgeführte CONSENSUS II (Studiennamen und Abkürzungen: siehe Tabelle 3), in der 6090 Patienten Enalapril (zuerst 1 mg intravenös, dann bis 20 mg/Tag per os) oder Placebo erhielten, wurde nach sechs Monaten vorzeitig abgebrochen wegen tendenziell (statistisch nicht signifikant) erhöhter Mortalität in der Enalaprilgruppe.(6)
In der GISSI-3-Studie, einer offenen Multizenterstudie, wurden 19’394 Patienten durch zweifache Randomisierung in vier Gruppen aufgeteilt: eine Placebogruppe, eine ACE-Hemmer-Gruppe (Lisinopril zuerst 5 mg, dann 10 mg täglich), eine Nitratgruppe und eine Gruppe mit Lisinopril plus Nitrat. Sechs Wochen nach Infarkt betrug die Mortalität der mit Lisinopril Behandelten 6,3% gegenüber 7,1% in der Placebogruppe. Dieser Unterschied ist statistisch signifikant.(7)
Ähnliche Resultate ergab die ISIS-4-Studie. In dieser offenen Multizenterstudie wurden Captopril (einschleichende Dosierung bis maximal 100 mg/Tag), Magnesium und ein Mononitrat an 58’050 Patienten geprüft. Nach fünf Wochen waren 7,2% der 29’000 mit Captopril behandelten Patienten gestorben, in der Kontrollgruppe war die Mortalität mit 7,7% signifikant höher.(8) Eine chinesische Studie, in der 13’634 Patienten innerhalb von 36 Stunden nach einem Herzinfarkt eine vierwöchige Therapie mit Captopril (bis 3mal 12,5 mg/Tag) oder Placebo begannen, hat nach vorläufiger Auswertung keine signifikante Senkung der Mortalität durch den ACE-Hemmer ergeben.(9)
Akutes Infarktstadium / Verwendung eines ACE-Hemmers bei Risikopatienten
Die SMILE-Studie umfasste 1556 Patienten mit akutem Vorderwandinfarkt, die für eine Thrombolyse nicht in Frage kamen. Sie erhielten innerhalb von 24 Stunden nach Schmerzbeginn doppelblind entweder Zofenopril, einen in der Schweiz bisher nicht verfügbaren ACE-Hemmer, oder Placebo. Die Behandlung wurde sechs Wochen lang durchgeführt. Nach einem Jahr Beobachtungszeit belief sich die Mortalität in der Zofenoprilgruppe auf 10,0%, in der Placebogruppe auf 14,1%. Diese Risikosenkung um 29% ist signifikant.(10)
Subakutes Infarktstadium / Verwendung eines ACE-Hemmers bei Risikopatienten
In die SAVE-Studie wurden 2231 Patienten mit asymptomatischer Dysfunktion des linken Ventrikels (Auswurffraktion 40% oder weniger) eingeschlossen, die drei bis 16 Tage vorher einen Myokardinfarkt erlitten hatten. Sie erhielten doppelblind während durchschnittlich 42 Monaten Captopril (bis 150 mg pro Tag) oder Placebo. Captopril senkte die Gesamtmortalität um 19%, die Zahl der durch Herzinsuffizienz verursachten Hospitalisationen um 22% und die Infarktrezidive um 25%. Die Mortalitätsreduktion erreichte aber erst nach 12 Monaten Behandlungszeit statistische Signifikanz. (11)
In der AIRE-Studie wurde Ramipril (5 bis 10 mg/Tag) bei Patienten mit klinisch manifester Herzinsuffizienz doppelblind mit Placebo verglichen. Die Randomisierung erfolgte 3 bis 10 Tage nach Infarkt. Nach 15 Monaten Studienzeit waren 23% in der Placebogruppe, aber nur 17% in der Ramiprilgruppe gestorben. Dies entpricht einer hochsignifikanten Risikosenkung um 27%, wobei die nutzbringende Wirkung bereits nach einem Monat ersichtlich war. Auch die Inzidenz der schweren Herzinsuffizienz wurde mit Ramipril signi- fikant vermindert. Die Zahl der Infarktrezidive war indessen in beiden Gruppen gleich hoch.(12)
In einer dänischen Multizenter-Doppelblindstudie (TRACE) wurde die Wirkung von Trandolapril (1 bis 4 mg/Tag) bei eingeschränkter linksventrikulärer Funktion (Auswurffraktion nicht grösser als 35%) mit oder ohne Zeichen einer Herzinsuffizienz untersucht. Insgesamt wurden 1749 Patienten 3 bis 7 Tage nach Herzinfarkt randomisiert und während 1 bis 4 Jahren behandelt. Trandolapril senkte die Mortalität gegenüber Placebo signifikant um 18%. In beiden Gruppen traten etwa gleich viele Infarktrezidive auf; eine progrediente Herzinsuffizienz wurde in der Trandolaprilgruppe dagegen signifikant seltener beobachtet.(13)
Chronisches Infarktstadium / Verwendung eines ACE-Hemmers bei Risikopatienten
Eine grosse placebokontrollierte Doppelblindstudie (SOLVD) umfasste 4218 Patienten mit asymptomatischer linksventrikulärer Dysfunktion (Auswurffraktion 35% oder weniger). In 80% der Fälle beruhte die Herzkrankheit auf einem vor mehr als 30 Tagen erlittenen Myokardinfarkt. Obwohl Enalapril (10 bis 20 mg täglich) die Inzidenz der Herzinsuffizienz gegenüber Placebo um 37% reduzierte, war die Gesamtmortalität nach drei Jahren Behandlungszeit in beiden Gruppen gleich hoch.(14)
Unerwünschte Wirkungen
Ein Blutdruckabfall kann im akuten Stadium eines Herzinfarktes zur Expansion der Nekrose und zu subendokardialen Ischämien führen. Das Hypotonierisiko scheint umso höher, je früher die Behandlung mit einem ACE-Hemmer begonnen wird. So musste Lisinopril in der GISSI-3-Studie bei rund 9% der Patienten wegen eines Abfalls des systolischen Blutdrucks auf unter 90 mm Hg abgebrochen werden.(7)
In CONSENSUS II, einer Studie, in der initial Enalaprilat intravenös gegeben wurde, fand sich gar bei 25% der Behandelten eine Hypotonie.(6) Demgegenüber trat nur in 4% der Fälle eine symptomatische Hypotonie auf, wenn die ACE-Hemmer-Behandlung wie in der AIRE-Studie erst einige Tage nach Schmerzbeginn eingeleitet wurde.(12)
Mit einer Abnahme der Nierenfunktion ist bei 2 bis 3% der Patienten zu rechnen. Diese grundsätzlich reversible Nebenwirkung wird durch Diuretika und nicht-steroidale Entzündungshemmer begünstigt. Besonders gefährdet sind Patienten mit einer Hyponatriämie.
Über einen trockenen Reizhusten klagen etwa 5% der Behandelten. Selten kommen Geschmacksstörungen, gastrointestinale Beschwerden, Exantheme und angioneurotische Ödeme vor.(15)
Schlussfolgerungen
Mit den ACE-Hemmern steht uns nun - neben den Thrombolytika, der Acetylsalicylsäure und den Betablockern - eine weitere Stoffklasse zur Verfügung, welche die Prognose von Patienten nach Myokardinfarkt verbessern kann. Die Experten sind sich jedoch über die Kriterien, nach denen die Indikation zur Verabreichung eines ACE- Hemmers zu stellen ist, und über den optimalen Zeitpunkt des Therapiebeginnes nicht einig.(16,17)
Sollen alle Patienten nach Herzinfarkt einen ACE-Hemmer erhalten? Die Senkung der Mortalität ist in den beiden sehr grossen Studien (GISSI-3, ISIS-4) zwar signifikant, aber doch zu gering ausgefallen, als dass die routinemässige Verabreichung eines ACE-Hemmers nach einem Herzinfarkt gerechtfertigt wäre. Es ist jedoch von grosser Bedeutung, möglichst rasch diejenigen Patienten zu identifizieren, welche am meisten von einem ACE- Hemmer profitieren. Hierzu kann man sich in erster Linie auf klinische Daten stützen, wenn Methoden zur Quantifizierung der linksventrikulären Funktion (Echokardiographie, Radionuklid-Ventrikulographie) nicht innerhalb von nützlicher Frist verfügbar sind. Bei Hinweisen auf einen ungünstigen Verlauf, namentlich Linksherzinsuffizienz, Infarktrezidiv, Vorderwandinfarkt, ST-Strecken-Hebung oder Q-Wellen in mehr als zwei EKG-Ableitungen, sollte ein ACE-Hemmer verabreicht werden, sobald sich der systolische Blutdruck bei Werten von mindestens 100 mm Hg stabilisiert hat, also in der Regel 12 bis 72 Stunden nach Spitaleintritt. Wird die Behandlung zu lange hinausgeschoben, so verringert sich der Nutzen einer ACE-Hemmer-Therapie.
Um das Risiko einer symptomatischen Hypotonie niedrig zu halten, empfiehlt es sich, die Behandlung mit einer kurzwirkenden Substanz in einer niedrigen Initialdosis (z.B. Captopril 6,25 mg) zu beginnen und vorgängig wenn möglich keine Diuretika zu verabreichen.
Im weiteren Verlauf (z.B. drei Monate nach Herzinfarkt) hilft die Bestimmung der linksventrikulären Auswurffraktion bei der Entscheidung, ob die Behandlung weitergeführt werden soll. Beträgt die Auswurffraktion 40% oder weniger, so ist die langfristige Verabreichung eines ACE-Hemmers angezeigt.
Zur Langzeitprophylaxe nach Myokardinfarkt sollten grundsätzlich nur adäquat dokumentierte Substanzen verwendet werden, und zwar in einer Dosis, die sich in grossen Studien als wirksam erwiesen hat.(11,12,13,18) Diesbezügliche Hinweise finden sich in Tabelle 4.
Kommentare
Bei der Behandlung von Patienten mit Myokardinfarkt haben die ACE-Hemmer einen festen Platz, wenn entweder eine klinisch manifeste Herzinsuffizienz und/oder eine wesentliche Einschränkung der linksventrikulären Funktion (Auswurffraktion unter 40%) vorliegen. Die heute vorliegenden Studien erlauben keine verbindlichen Aussagen über den optimalen Zeitpunkt des Therapiebeginns. Bei einem Früheinsatz in den ersten 24 Stunden nach Schmerzbeginn kann die Mortalität signifikant gesenkt werden. Wegen der möglichen Nebenwirkungen (vor allem arterielle Hypotonie) und wegen des nur mässigen absoluten Nutzens (Beispiel ISIS-4: auf 1000 behandelte Patienten wurden 5 Todesfälle vermieden) hat der routinemässige Früheinsatz bis heute keine generelle Akzeptanz gefunden. Da sich über 70% der Frühtodesfälle in den ersten drei bis fünf Tagen ereignen (GISSI-3 und ISIS-4), sollte der Einsatz von ACE-Hemmern bei den vorgenannten Risikopatienten möglichst rasch nach der hämodynamischen Stabilisierung (in der Regel am zweiten oder dritten Hospitalisationstag) erfolgen.
Auch wenn die Resultate der verschiedenen Studien mit verschiedenen Präparaten in die gleiche Richtung weisen und damit ein Klasseneffekt der ACE-Hemmer angenommen werden kann, empfiehlt sich grundsätzlich der Einsatz von Medikamenten mit guter Studiendokumentation. Solange keine Daten betreffend Dosis-Wirkungsbeziehung der ACE-Hemmer nach Myokardinfarkt vorliegen, muss empfohlen werden, Zieldosis und Dosierungsintervall gemäss den einzelnen Studienprotokollen zu handhaben.
W. Angehrn
Die Geschichte der Entwicklung und Anwendung der ACEHemmer im klinischen Bereich stellt ein vorbildliches Beispiel für das Prinzip «from bench to bedside» dar.
Während den letzten 15 Jahren hat man die vielfältige pathophysiologische und biologische Bedeutung dieser Substanzen erkannt («bench»). ACE-Hemmer führen zu einer Senkung der Vor- und Nachlastbelastung des linken Ventrikels und damit zu einer Verbesserung der Sauerstoffversorgung bzw. einer Senkung des myokardialen Sauerstoffverbrauchs. Angiotensin II beeinflusst die Expression bestimmter Protoonkogene, die ihrerseits für die Ausbildung einer Myokard-Hypertrophie verantwortlich sind. Angiotensin II spielt anderseits auch eine wichtige Rolle bei der Pathogenese der Atherosklerose. ACE-Hemmer reduzieren die neurohumorale Stimulation sowohl im Tierversuch als auch im klinischen Experiment. Gemäss verschiedenen Untersuchungen sind Personen mit einer (polymorph determinierten) Variante des ACE-Gens (ACE-DD) signifikant mehr gefährdet, einen Herzinfarkt zu erleiden, als Vergleichspersonen.
Die in der vorliegenden Übersicht vorgestellten Studien stellen das klinische Korrelat der ACE-Hemmer-Story dar («bedside »). Sie zeigen, dass diese Medikamente einerseits die Infarktmortalität senken können, anderseits aber auch eine günstige Wirkung auf das Manifestwerden einer Herzinsuffizienz und auf Infarktrezidive ausüben.
Literatur
- 1) Multicenter Postinfarction Research Group. N Engl J Med 1983; 309:331-6
- 2) Pfeffer MA. Ann Rev Med 1995; 46: 455-66
- 3) Maurer E. pharma-kritik 1991; 13: 77-80
- 4) Garb R, Yusuf S. JAMA 1995; 273: 1450-6
- 5) Konstam MA et al. Circulation 1992; 86: 431-8
- 6) Swedberg K et al. N Engl J Med 1992; 327: 678-84
- 7) Gruppo Italiano per lo studio della Sopravvivenza nell' Infarto Miocardico (GISSI-3). Lancet 1994; 343: 1115-22
- 8) ISIS-4 Collaborative Group. Lancet 1995; 345: 669-85
- 9) Lisheng L et al. Lancet 1995; 345: 386-7
- 10) Ambrosioni E et al. N Engl J Med 1995; 332: 80-5
- 11) Pfeffer MA et al. N Engl J Med 1992; 327: 669-77
- 12) The Acute Infarction Ramipril Efficacy Study Investigators (AIRE). Lancet 1993; 342: 821-8
- 13) Kober L et al. N Engl J Med 1995; 333: 1670-6
- 14) SOLVD Investigators. N Engl J Med 1992; 327: 685-91
- 15) Kostis JB et al. Am Heart J 1996; 131: 350-5
- 16) Ball SG. et al. J Am Coll Cardiol 1995; 25 (Suppl): 42S-46S
- 17) Coats AJ. Br Heart J 1995; 73: 395-6
- 18) SOLVD Investigators. N Engl J Med 1991; 325: 293-302
Standpunkte und Meinungen
- Es gibt zu diesem Artikel keine Leserkommentare.
Copyright © 2024 Infomed-Verlags-AG
PK442
Gratisbuch bei einem Neuabo!
pharma-kritik abonnieren
-
Jahrgang 45 / 2023
Jahrgang 44 / 2022
Jahrgang 43 / 2021
Jahrgang 42 / 2020
Jahrgang 41 / 2019
Jahrgang 40 / 2018
Jahrgang 39 / 2017
Jahrgang 38 / 2016
Jahrgang 37 / 2015
Jahrgang 36 / 2014
Jahrgang 35 / 2013
Jahrgang 34 / 2012
Jahrgang 33 / 2011
Jahrgang 32 / 2010
Jahrgang 31 / 2009
Jahrgang 30 / 2008
Jahrgang 29 / 2007
Jahrgang 28 / 2006
Jahrgang 27 / 2005
Jahrgang 26 / 2004
Jahrgang 25 / 2003
Jahrgang 24 / 2002
Jahrgang 23 / 2001
Jahrgang 22 / 2000
Jahrgang 21 / 1999
Jahrgang 20 / 1998
Jahrgang 19 / 1997
Jahrgang 18 / 1996
Jahrgang 17 / 1995
Jahrgang 16 / 1994
Jahrgang 15 / 1993
Jahrgang 14 / 1992
Jahrgang 13 / 1991
Jahrgang 12 / 1990
Jahrgang 11 / 1989
Jahrgang 10 / 1988
Kennen Sie "100 wichtige Medikamente" schon?
Die Liste der 100 Medikamente sehen Sie auf der Startseite von 100 Medikamente.