Gicht
- Autor(en): Alex Flückiger
- Reviewer: Pius Brühlmann, Ivo Büchler, Karin Fattinger, Dieter Frey
- pharma-kritik-Jahrgang 28
, Nummer 13, PK164
Redaktionsschluss: 29. März 2007
DOI: https://doi.org/10.37667/pk.2006.164 - PDF-Download der Printversion dieser pharma-kritik Nummer
Update
Die Gicht ist die häufigste entzündliche Gelenkerkrankung bei Männern über vierzig Jahren. Frauen sind drei- bis sechsmal seltener betroffen; das erstmalige Auftreten einer Gicht nach dem 60. Altersjahr ist aber bei Frauen und Männern gleich häufig. Die Krankheit steht in enger Beziehung zur Harnsäure- Plasmakonzentration. In einer 1987 veröffentlichten Kohortenstudie, an der 2046 zuvor gesunde Männer teilnahmen, erkrankten bei Harnsäure-Plasmakonzentrationen von unter 416 µmol/l jährlich 0,09%, innert 5 Jahren 0,6% der Teilnehmer an Gicht. Die entsprechenden Prozentzahlen betrugen 0,5% bzw. 3% bei Konzentrationen von 416 bis 536 µmol/l, 4,9% bzw. 22% bei Konzentrationen von 536 bis 595 µmol/l und 7% bzw. 30,5% bei Konzentrationen von über 595 µmol/l.(1) Darob sollte man jedoch nicht vergessen, dass nur eine Minderheit der Personen mit Hyperurikämie jemals einen Gichtanfall erleidet: In industrialisierten Ländern findet sich eine Hyperurikämie bei rund 20% der erwachsenen Männer, eine Gicht jedoch «nur» bei knapp 2%.
Pathogenese
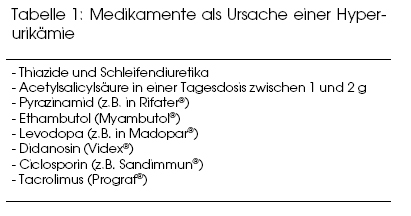
Harnsäure entsteht als schwer wasserlösliches Endprodukt des Purinstoffwechsels hauptsächlich in der Leber, in geringem Mass auch in der Dünndarmmukosa. Im Gegensatz zu den meisten Tieren fehlt dem Menschen das Enzym Uratoxidase, das Harnsäure zum hydrophilen – leicht eliminierbaren – Allantoin abbaut, so dass die Ausscheidung Probleme bereitet und vergleichsweise hohe Harnsäure-Plasmaspiegel bestehen. Die Elimination erfolgt zu rund 75% über die Nieren: Glomerulär filtrierte Harnsäure wird durch ein im proximalen Tubulus gelegenes Transportsystem, den «Uric Acid Transporter 1» (URAT1), im Austausch gegen andere Anionen praktisch vollständig rückresorbiert,(2) gefolgt von proximal tubulärer Sekretion und erneuter Rückresorption.Die primäre Hyperurikämie/Gicht beruht in 90% auf einer polygen festgelegten Verminderung der renalen Harnsäure- Elimination und in 10% auf einer idiopathischen Harnsäureüberproduktion. Zudem kennt man vier äusserst seltene kongenitale Enzymdefekte, die mit gesteigerter Purinsynthese verbunden sind, unter ihnen der Hypoxanthin-Guanin-Phosphoribosyltransferase- Mangel beim Lesch-Nyhan-Syndrom und die Phosphoribosylpyrophosphat-Synthetase-Überaktivität.Die sekundäre Hyperurikämie/Gicht wird einerseits durch eine verminderte renale Harnsäureausscheidung bei Niereninsuffizienz, polyzystischer Nierenerkrankung, Bleivergiftung, arterieller Hypertonie, Insulinresistenz, Sarkoidose, Diabetes insipidus, Hypothyreose, Hyperparathyreoidismus, Ketoazidose, Laktatazidose und als unerwünschte Wirkung von Medikamenten (siehe Tabelle 1) verursacht, andererseits durch eine vermehrte Harnsäureproduktion bei myeloproliferativen, lymphoproliferativen und anderen neoplastischen Erkrankungen, bei hämolytischer Anämie, Perniziosa und Psoriasis.(3) Bei Adipositas und übermässigem Alkoholkonsum kommen beide Mechanismen zum Tragen.
Bis zu einer Konzentration von etwa 400 µmol/l liegt die Harnsäure in extrazellulären Flüssigkeiten in gelöster Form vor,
oberhalb dieses Wertes besteht eine gesättigte Lösung mit einer Tendenz zur Ausfällung von Mononatrium-Urat-Kristallen (MSU-Kristallen). Niedrige pH-Werte, Dehydratation, tiefe Temperaturen und Gelenkknorpelschäden begünstigen die lokale Kristallbildung. Damit lässt sich die bevorzugte Ablagerung von MSU-Kristallen im biomechanisch besonders belasteten Grosszehengrundgelenk erklären, wo verhältnismässig kühle Temperaturen herrschen und degenerative Veränderungen oft schon in jüngeren Jahren auftreten.
Die in der Synovialflüssigkeit abgelagerten MSU-Kristalle bilden mit Immunglobulinen, Apolipoproteinen und anderen
Eiweissen Komplexe, die sich an Oberflächenrezeptoren von Mastzellen und Monozyten binden und phagozytiert werden. Dies bewirkt eine Freisetzung von Zytokinen und chemotaktischen Faktoren und einen ausgiebigen Zustrom von neutrophilen Granulozyten, die sich an der Phagozytose der Kristalle beteiligen und weitere Entzündungsmediatoren freisetzen.(3,4) Die Prozesse, die zur spontanen Rückbildung des Gichtanfalls führen, sind komplex. Wichtige Funktionen haben ausgereifte Makrophagen und enzündungshemmende Mediatoren, etwa der Interleukin-1-Rezeptor-Antagonist.(3)
Klinik und Diagnostik
Die akute Gicht ist charakterisiert durch eine plötzlich und typischerweise nachts auftretende, überaus schmerzhafte Monarthritis oder Oligarthritis, die meistens die peripheren Gelenke der unteren Extremitäten betrifft. In rund der Hälfte aller Fälle ist das Grosszehengrundgelenk beteiligt. Oft werden systemische Entzündungszeichen (Fieber, Leukozytose, CRP-Erhöhung) beobachtet. Unbehandelt klingt der Gichtschub in 1 bis 2 Wochen langsam ab. Extraartikuläre Manifestationen (Bursitis, Tendovaginitis) und polyartikuläre Formen sind seltener. Bei bis zu 10% der von einer Gichtattacke betroffenen Personen ist der Harnsäure-Plasmaspiegel in der akuten Phase normal. Die Diagnose sollte mittels Punktion eines betroffenen Gelenkes gesichert werden. Damit kann auch eine infektiöse Arthritis, die wichtigste Differentialdiagnose, mittels Gramfärbung und Kultur ausgeschlossen werden. Der Gelenkerguss ist bei einem Gichtanfall entzündlich, mit Leukozytenzahlen von über 10’000/µl und einem starkem Überwiegen der neutrophilen Granulozyten. Der mikroskopische Nachweis von intrazellulären MSU-Kristallen sichert die Diagnose. Extrazelluläre Kristalle können bei Personen mit einer Gicht auch in nichtgichtbedingten Gelenkergüssen nachgewiesen werden. Radiologische Untersuchungen und die Messung der Harnsäure- Ausscheidung im 24-Stunden-Urin sind zur Diagnose einer akuten Gicht nicht notwendig. Zur Erfassung der häufigsten Ursachen einer sekundären Gicht sollte nach dem Abklingen der akuten Phase ein Differentialblutbild angefertigt und – besonders bei Frauen vor der Menopause – die Nieren- und Schilddrüsenfunktion untersucht werden.
Der erste Gichtanfall heilt in der Regel ohne Residuen ab, Rezidive sind jedoch häufig. In einer vor der Allopurinol-Ära
durchgeführten Studie erlitten innert zwei Jahren 78% der Teilnehmenden, innert zehn Jahren 93% eine zweite Attacke. Auch werden die symptomfreien Intervalle bei vielen unbehandelten Personen immer kürzer, bis schliesslich nach durchschnittlich zwölf Jahren eine chronische Gicht vorliegt.
Die chronische tophöse Gicht hat mit der Einführung von Allopurinol stark an Bedeutung verloren. Ihre häufigste Manifestation ist eine langsam progrediente, in der Regel polyartikuläre Synovitis, die oft mit Tophusbildung in und an den Gelenken einhergeht und zu radiologisch nachweisbaren Gelenk- und Knochendestruktionen führt. Subkutane Tophi – derbe, verschiebbare, aus MSU-Kristallen bestehende Knötchen – finden sich vor allem in der Nähe von Gelenken, aber auch in der Ohrmuschel und, wenn auch höchst selten, in viszeralen Organen. Im Rahmen einer Gichtattacke können sie schmerzhaft werden, ulzerieren und sich sekundär infizieren. Tophi sind unter Allopurinol reversibel.
Assoziierte Erkrankungen
Der enge Zusammenhang von Hyperurikämie und arterieller Hypertonie ist gut belegt; er beruht auf einer Verminderung
der renalen Harnsäure-Exkretion bei erhöhten Blutdruckwerten. (5,6) Auch zum metabolischen Syndrom besteht eine starke Assoziation.(7) Ob eine Hyperurikämie oder Gicht einen unabhängigen Risikofaktor für die koronare Herzkrankheit darstellt, ist indes umstritten.(8,9)
Harnsäuresteine treten bei Gicht gehäuft auf, vor allem wenn diese mit einer Hyperurikosurie verbunden ist. Beträgt die Uratausscheidung im Urin bei einem Gichtkranken weniger als 600 mg/24 h, ist bei etwa 20% mit einer Urolithiasis zu rechnen; beträgt sie mehr als 1000 mg/24 h, so steigt das Risiko auf 50% an. Auch ein Urin-pH-Wert von weniger als 5,5 begünstigt die Steinbildung.
Viele Fachleute bezweifeln, dass die chronische Uratnephropathie (Gichtniere) im engeren Sinn, eine durch Ablagerung von Tophi verursachte und mit zunehmender Niereninsuffizienz einhergehende tubulointerstitielle Erkrankung, als klinische Entität bedeutsam ist.(3) Den meisten Fällen von gichtassoziierter Niereninsuffizienz liegt wahrscheinlich eine unabhängige – die Uratelimination beeinträchtigende – Nierenerkrankung, z.B. eine hypertensive Nephropathie, zu Grunde. Aus renaler Sicht ist somit eine isolierte Hyperurikämie allein nicht behandlungsbedürftig.
Behandlung des Gichtanfalls
Die Behandlung des Gichtanfalls basiert weniger auf Evidenz als auf praktischen Erfahrungen.(10) Erste Wahl ist die hoch dosierte und möglichst frühzeitige Verabreichung eines nichtsteroidalen Entzündungshemmers, unterstützt durch Ruhigstellung und Kühlung des betroffenen Gelenks und durch reichliche Flüssigkeitszufuhr zur Steigerung der Harnsäureausscheidung. Am besten dokumentiert ist Indometacin (z.B. Indocid®, bis 150 mg/Tag), das jedoch häufig Nebenwirkungen verursacht. Als wahrscheinlich gleichwertige und etwas besser verträgliche Alternativen stehen Ibuprofen (z.B. Brufen®, bis 2400 mg/Tag), Naproxen (z.B. Proxen®, maximal 1250 mg/Tag), Diclofenac (z.B. Voltaren®, bis 150 mg/Tag), Etodolac (Lodine®, maximal 1200 mg/Tag), Acemetacin (Tilur®, bis 180 mg/Tag) und Piroxicam (z.B. Felden®, bis 40 mg/Tag) zur Verfügung. Die verschiedenen Substanzen sind bisher allerdings nicht direkt miteinander verglichen worden.(11) Sobald die Schmerzen abgeklungen sind, kann das Medikament innert weniger Tage ausgeschlichen werden.
Kortikosteroide, intraartikulär und/oder systemisch verabreicht, haben in den letzten Jahren einen grösseren Stellenwert in der Gichttherapie erhalten, ohne dass ihre Wirkung in aussagekräftigen Studien untersucht worden wäre.(12) Bei intraartikulärer Anwendung sollte der Erguss möglichst vollständig entleert werden, bevor ein lang wirkendes Kortikosteroid wie Triamcinolon (z.B. Kenacort A®) in einer der Gelenksgrösse angepassten Dosis – 5 bis 10 mg für das Metatarsophalangealgelenk, 20 bis 40 mg für das Sprunggelenk, 40 mg für das Kniegelenk – injiziert wird. Die orale Verabreichung von Prednisolon oder Prednison (Startdosis 30 bis 60 mg/Tag während 2 bis 3 Tagen, dann Ausschleichen über 10 bis 14 Tage) ist in der Regel polyartikulären Erscheinungsformen sowie Fällen, in denen nichtsteroidale Entzündungshemmer kontraindiziert sind oder ungenügend wirken, vorbehalten.
Colchicin, ein Mitosehemmstoff aus dem Gift der Herbstzeitlosen, wirkt entzündungshemmend, indem es Migration und
Funktion (Phagozytose und Freisetzung von Entzündungsvermittlern) der neutrophilen Granulozyten hemmt. Es wird vorwiegend hepatisch eliminiert. Dieses Medikament weist eine geringe therapeutische Breite auf und zeichnet sich durch seine ausgeprägte gastrointestinale Toxizität – ein dosisabhängig auftretender und oft von Bauchschmerzen begleiteter Durchfall – aus. Colchicin sollte deshalb nur noch ausnahmsweise bei Kontraindikationen oder Unverträglichkeit der Standardtherapie zum Einsatz gelangen. Offiziell ist in der Schweiz kein Fertigpräparat mehr erhältlich, ein solches kann jedoch z.B. aus Deutschland (Colchicum-Dispert®-Tabletten, Colchysat®- Lösung) beschafft werden. Das rasche Ansprechen auf Colchicin ist typisch, aber nicht beweisend für Gicht – auch andere Kristallerkrankungen wie die Chondrokalzinose (Pyrophosphatablagerungs- Krankheit) reagieren auf Colchicin.
Nachdem Colchicin während langer Zeit in hohen Dosen verabreicht worden ist (als Standard galt eine Startdosis von 1 mg, gefolgt von 0,5 mg alle 2 bis 3 Stunden, bis zur Schmerzfreiheit oder zum Auftreten von unerwünschten Wirkungen bzw. bis zu einer Gesamtdosis von 6 mg pro Anfall), wird heute – rein empirisch – eine vergleichsweise niedrige Dosis von 0.5 mg alle 8 Stunden während maximal 4 Tagen empfohlen.(13) Bei Lebererkrankungen und fortgeschrittener Niereninsuffizienz ist Colchicin kontraindiziert. Colchicin ist ein Substrat des Transportproteins P-Glykoprotein und des Zytochrom-Isoenzyms CYP3A4, weshalb es zu gefährlichen Interaktionen z.B. mit Makrolid-Antibiotika, Ciclosporin (z.B. Sandimmun®) und Statinen Anlass geben kann. Gemäss einer retrospektiven Studie starben 10% der gleichzeitig mit Colchicin und Clarithromycin (z.B. Klacid®) behandelten Personen.(14)
Langzeitbehandlung der Gicht
Ziele der Langzeitbehandlung sind die Verhütung von Gichtanfällen und die Normalisierung der Harnsäure-Konzentrationen im Plasma und Gewebe, so dass Gichttophi und Uratnierensteine kleiner werden oder verschwinden. Gewichtsreduktion, Einschränkung des Verzehrs von Fleisch und Meeresfrüchten zu Gunsten von Milchprodukten, Verzicht auf alkoholische Getränke (besonders auf Bier und Schnaps; massvoller Weingenuss scheint die Gichtanfälligkeit nicht zu erhöhen)(15) und, wenn möglich, das Absetzen von Medikamenten, die den Harnsäurespiegel erhöhen, sind die wichtigsten nichtmedikamentösen Massnahmen zur Gichtprävention. Purinreiche Gemüse haben wahrscheinlich keinen Einfluss auf die Gichthäufigkeit.(16)
Bei Uratnephrolithiasis sollte der Urin-pH-Wert mit Kaliumzitrat (4 bis 6 Kalium-Hausmann®-Effervetten, entsprechend einer Zitratdosis von 60 bis 90 mmol pro Tag) auf mindestens 6,2 angehoben werden. Von der Verabreichung eines
Natriumbikarbonat-Präparats wird abgeraten, da die vermehrte Natriumzufuhr die Entstehung von Kalziumoxalatsteinen
begünstigt.
In den ersten Monaten einer Behandlung mit Allopurinol oder einem Urikosurikum wird Harnsäure aus den betroffenen Gelenken mobilisiert, sodass vermehrt Gichtanfälle auftreten können. Um dies zu verhindern, sollte nach einem Gichtanfall mit der Behandlung mindestens 6 Wochen zugewartet und dann mit einer niedrigen Dosis (z.B. 100 mg Allopurinol täglich) begonnen werden. Auch die prophylaktische Gabe eines nichtsteroidalen Entzündungshemmers (z.B. Naproxen, 2-mal 250 mg/Tag) oder allenfalls von Colchicin (0,5 bis 1 mg/Tag) während 3 bis 6 Monaten ist zu erwägen. Die langfristige Verabreichung von Colchicin birgt allerdings das Risiko von hämatologischen Störungen sowie einer Alopezie, Azoospermie und Myopathie in sich und erfordert regelmässige Kontrollen der Serum-Kreatininphosphokinase und des Blutbilds.
Allopurinol
Allopurinol (z.B. Zyloric®, mit einer Halbwertszeit von 1 Stunde) und sein Hauptmetabolit Oxipurinol (Halbwertszeit 14 bis
30 Stunden) hemmen die Xanthinoxidase und damit die Umwandlung von Hypoxanthin zu Xanthin und von Xanthin zu
Harnsäure – die Harnsäure-Plasmakonzentration nimmt ab. Darüber hinaus wird die Ausscheidung der Oxypurine Hypoxanthin und Xanthin im Urin gesteigert, die somit in geringerer Menge für die Neusynthese von Purinen zur Verfügung stehen. Wenngleich Allopurinol bis heute, vierzig Jahre nach seiner Einführung, in keiner einzigen placebokontrollierten Doppelblindstudie untersucht worden ist, ist sein Stellenwert in der Gichtbehandlung unbestritten, unabhängig davon, ob eine verminderte Harnsäureelimination oder eine vermehrte Harnsäureproduktion zu Grunde liegt.(10,11) Die Indikation zur langfristigen Verabreichung ist gegeben, wenn pro Jahr mindestens zwei bis drei Gichtanfälle auftreten, bei Gichttophi, bei typischen radiologischen Gelenksveränderungen, bei rezidivierender Uratnephrolithiasis und bei einer Uratnephropathie. 9 Bei asymptomatischer Hyperurikämie ist ein Nutzen von Allopurinol bislang nicht belegt. Einzelne Experten raten trotzdem zur Behandlung, wenn der Harnsäure-Plasmaspiegel 600 µmol/l übersteigt, insbesondere wenn gleichzeitig eine ausgeprägte Hyperurikosurie (über 1000 mg/24 h) mit entsprechend hohem Nierensteinrisiko vorliegt. Allopurinol hat auch in der Hyperurikämie-Prophylaxe bei Chemo- und Radiotherapie von lympho- oder myeloproliferativen Erkrankungen einen gesicherten Platz.
Um die Harnsäure-Plasmakonzentration auf den Zielwert von unter 360 µmol/l zu senken, sind – individuell ermittelte – Tagesdosen von 100 bis 600 mg, ausnahmsweise bis 900 mg notwendig. Tagesdosen von über 300 mg werden besser auf mehrere Einzelgaben verteilt. Da Allopurinol und Oxipurinol ausschliesslich renal ausgeschieden werden, sollte die Dosis der Nierenfunktion angepasst werden. Empfohlen wird eine Tagesdosis von maximal 200 mg bei einer Kreatininclearance von 60 bis 80 ml/min, von maximal 150 mg bei 40 bis 60 ml/min und von maximal 100 mg bei 20 bis 40 ml/min. Liegt die Kreatininclearance unter 20 ml/min, sollte das Dosisintervall auf 48 bis 72 Stunden verlängert werden.
Bei 5 bis 10% muss die Behandlung aufgrund von unerwünschten Wirkungen abgebrochen werden. Am häufigsten sind dosisabhängig auftretende makulopapulöse und urtikarielle Exantheme; sie erfordern ein sofortiges Absetzen von Allopurinol, da sie – namentlich bei Personen mit Niereninsuffizienz und bei solchen, die ein Thiaziddiuretikum einnehmen – in ein lebensbedrohliches Überempfindlichkeitssyndrom mit exfoliativer Dermatitis, Hepatitis, interstitieller Nephritis, Vaskulitis, Knochenmarkdepression und Eosinophilie ausufern können. Hepatotoxische Reaktionen und Blutbildveränderungen können auch isoliert auftreten. Gelegentlich werden gastrointestinale Beschwerden beobachtet.
Die Dosis der Purinanaloga Azathioprin (z.B. Imurek®) und Mercaptopurin (Puri-Nethol®), die durch die Xanthinoxidase inaktiviert werden, sollte bei gleichzeitiger Verabreichung von Allopurinol auf 25% reduziert werden. Andere Interaktionen
(Verstärkung der Wirkung von oralen Antikoagulantien, Ciclosporin und Theophyllin) sind von fraglicher klinischer Relevanz. Aminopenicilline wie Amoxicillin (z.B. Clamoxyl®) erhöhen wahrscheinlich das Exanthemrisiko unter Allopurinol.
Urikosurika
Probenecid (Santuril®, teilbare Tabletten zu 500 mg) ist heute das einzige Urikosurikum, das in der Schweiz erhältlich ist. Es hemmt kompetitiv die tubuläre Rückresorption von Harnsäure und steigert so die Harnsäure-Exkretion, was initial das Risiko von Nierensteinen erhöht. Die Verwendung von Probenecid (Beginn mit 2-mal 250 mg/Tag während einer Woche, dann Steigerung auf 1 bis 2 g/Tag, verteilt auf 2 bis 4 Dosen) kann bei Allopurinol-Unverträglichkeit in Betracht gezogen werden, sofern keine Urolithiasis vorliegt, die Nierenfunktion normal ist und die Harnsäure im 24-Stunden-Urin 800 mg nicht überschreitet. Besondere Aufmerksamkeit muss auf eine reichliche Flüssigkeitszufuhr (mindestens 2 Liter pro Tag) gerichtet werden. Eine Kombination mit Allopurinol ist grundsätzlich möglich, aber kaum je notwendig.
Gastrointestinale Störungen, Exantheme, Gingivitis und Alopezie sind die häufigsten unerwünschten Wirkungen von Probenecid. Einzelfälle von Anaphylaxie, Hepatopathie, nephrotischem Syndrom, exfoliativer Dermatitis und Blutbildveränderungen sind beschrieben. Probenecid beeinflusst die proximal tubuläre Sekretion und erhöht deshalb die Plasmaspiegel zahlreicher Medikamente, die über diesen Mechanismus eliminiert werden – namentlich jene der Betalaktam-Antibiotika, Chinolone, Tuberkulostatika, Virustatika, Sulfonylharnstoffe, nichtsteroidalen Entzündungshemmer und von Methotrexat. Acetylsalicylsäure und Pyrazinamid (in Rifater® u.a.) hemmen die Wirkung von Probenecid.
Andere Medikamente
Eine Reihe von kleinen Studien hat gezeigt, dass Amlodipin (z.B. Norvasc®), Losartan (Cosaar®) und die Lipidsenker Atorvastatin (Sortis®) und Fenofibrat (Lipanthyl®) die Harnsäure- Plasmakonzentration aufgrund ihrer urikosurischen Wirkung um bis zu 20% vermindern.(17) Ferner ergab eine Doppelblindstudie mit 184 Teilnehmenden, die während 2 Monaten Vitamin C (500 mg/Tag) oder Placebo erhielten, für die aktiv behandelte Gruppe eine statistisch signifikante Abnahme der Plasma-Harnsäurekonzentration um 30 µmol/l.(18) Bisher gibt es jedoch keine Daten, die eine Reduktion von Gichtanfällen durch die langfristige Verabreichung einer dieser Substanzen belegen würden.
Febuxostat, ein neuer, bisher noch nicht zugelassener Xanthinoxidase- Hemmer, wurde in einer Doppelblindstudie in zwei verschiedenen Dosen während 52 Wochen mit Allopurinol verglichen. Der primäre Endpunkt, ein Harnsäure-Plasmaspiegel von weniger als 360 µmol/l, wurde mit beiden Febuxostat- Dosen (80 bzw. 120 mg/Tag) signifikant häufiger erreicht als mit Allopurinol (300 mg/Tag). Die Behandlung wurde jedoch in den beiden Febuxostat-Gruppen signifikant häufiger abgebrochen (vorwiegend wegen unerwünschten Wirkungen oder Gichtschüben) als in der Allopurinol-Gruppe; zudem ereigneten sich in der Febuxostat-Gruppe 4 Todesfälle.(19)
Die rekombinante Uratoxidase Rasburicase (Fasturtec®) ist bisher einzig zur intravenösen Prophylaxe und Therapie des sogenannten Tumorlysesyndroms (Ausfällung von Harnsäurekristallen in den Nierentubuli bei der Chemotherapie von akuten
Leukämien und Lymphomen) zugelassen. Sie katalysiert die Oxidation von Harnsäure zu Allantoin, einer wasserlöslichen Substanz, die leicht über die Nieren ausgeschieden wird, so dass sich der Harnsäure-Plasmaspiegel innert weniger Stunden normalisiert.(20) Eine pegylierte – für die Anwendung bei therapierefraktärer Gicht entwickelte – Form steht derzeit in klinischer Prüfung.(21)
Literatur
- 1) Campion EW et al. Am J Med 1987; 82: 421-6
- 2) Enomoto A et al. Nature 2002; 417: 447-52
- 3) Choi HK et al. Ann Intern Med 2005; 143: 499-516
- 4) Suresh E. Postgrad Med J 2005; 81: 572-9
- 5) Choi HK et al. Arch Intern Med 2005; 165: 742-8
- 6) Janssens HJ et al. Fam Pract 2003; 20: 413-6
- 7) Kahn HS et al. Am J Clin Nutr 2003; 78: 928-34
- 8) Baker JF et al. Am J Med 2005; 118: 816-26
- 9) Saag KG, Mikuls TR. Curr Rheumatol Rep 2005; 7: 235-41
- 10) Schlesinger N. Drugs 2004; 64: 2399-2416
- 11) Underwood M. Br Med J 2006; 332: 1315-9
- 12) Mikuls TR, Saag KG. Curr Rheumatol Rep 2005; 7: 242-9
- 13) Morris I et al. Br Med J 2003; 327: 1275-6
- 14) Hung IF et al. Clin Infect Dis 2005; 41: 291-300
- 15) Choi HK et al. Lancet 2004; 363: 1277-81
- 16) Choi HK et al. N Engl J Med 2004; 350: 1093-103
- 17) Lee SJ, Terkeltaub RA.: Curr Rheumatol Rep 2006; 8: 224-30
- 18) Huang HJ et al. Arthritis Rheum 2005; 52: 1843-7
- 19) Becker MA et al. N Engl J Med 2005; 353; 2450-61
- 20) Oldfield V, Perry CM. Drugs 2006; 66: 529-45
- 21) Bieber JD, Terkeltaub RA. Arthritis Rheum 2004; 50: 598-606
Standpunkte und Meinungen
- Es gibt zu diesem Artikel keine Leserkommentare.
Copyright © 2024 Infomed-Verlags-AG
PK164
Verwandte Artikel
LoginGratisbuch bei einem Neuabo!
pharma-kritik abonnieren
-
Jahrgang 45 / 2023
Jahrgang 44 / 2022
Jahrgang 43 / 2021
Jahrgang 42 / 2020
Jahrgang 41 / 2019
Jahrgang 40 / 2018
Jahrgang 39 / 2017
Jahrgang 38 / 2016
Jahrgang 37 / 2015
Jahrgang 36 / 2014
Jahrgang 35 / 2013
Jahrgang 34 / 2012
Jahrgang 33 / 2011
Jahrgang 32 / 2010
Jahrgang 31 / 2009
Jahrgang 30 / 2008
Jahrgang 29 / 2007
Jahrgang 28 / 2006
Jahrgang 27 / 2005
Jahrgang 26 / 2004
Jahrgang 25 / 2003
Jahrgang 24 / 2002
Jahrgang 23 / 2001
Jahrgang 22 / 2000
Jahrgang 21 / 1999
Jahrgang 20 / 1998
Jahrgang 19 / 1997
Jahrgang 18 / 1996
Jahrgang 17 / 1995
Jahrgang 16 / 1994
Jahrgang 15 / 1993
Jahrgang 14 / 1992
Jahrgang 13 / 1991
Jahrgang 12 / 1990
Jahrgang 11 / 1989
Jahrgang 10 / 1988
Kennen Sie "100 wichtige Medikamente" schon?
Die Liste der 100 Medikamente sehen Sie auf der Startseite von 100 Medikamente.