Plasmaersatzstoffe
- Autor(en): Urspeter Masche
- Reviewer: Ulrich F. Gruber, Joseph Osterwalder, Hansjürg Schaer, Bruno Tschirren
- pharma-kritik-Jahrgang 12
, Nummer 01, PK579
Redaktionsschluss: 14. Januar 1990 - PDF-Download der Printversion dieser pharma-kritik Nummer
Übersicht
Jede grössere Abnahme des zirkulierenden Blutvolumens gefährdet die Vitalfunktionen. Eine absolute Hypovolämie tritt bei Blut-, Plasma- oder reinen Flüssigkeitsverlusten auf; eine relative Hypovolämie manifestiert sich z.B. beim anaphylaktischen Schock, wenn -- bei normalem Blutvolumen -- das Schlagvolumen des Herzens wegen des erniedrigten Venentonus absinkt.
Ein Volumenersatz wird in erster Linie mit kristalloiden und kolloidalen Lösungen durchgeführt. Als kristalloide Lösungen bezeichnet man die reinen Elektrolytlösungen. Kolloidale Lösungen enthalten ein Makromolekül, das in der Blutbahn einen kolloid-osmotischen bzw. onkotischen Druck erzeugt. Sobald der Hämatokrit unter einen kritischen Wert fällt (bei älteren Personen 0,30, bei jüngeren, ansonsten gesunden etwa 0,20), müssen Erythrozyten mittransfundiert werden. Je nach klinischer Situation wird man auch andere Plasma- oder Blutkomponenten verabreichen. Aus gespendetem Blut hergestellte Infusionen sollten aber zurückhaltend gebraucht werden, denn sie sind teuer, nur beschränkt verfügbar und können -- sofern nicht sterilisierbar -- Infektionen übertragen.
Kristalloide
Für den Volumenersatz verwendete Elektrolytlösungen sind die 0,9%ige Kochsalzlösung und die Ringer-Lösungen. Die 0,9%ige Kochsalzlösung enthält eine hohe Chloridkonzentration (154 mmol/l), was theoretisch das Säure- Basen-Gleichgewicht verschieben kann. Die Ringer-Lösungen sind in bezug auf den Elektrolytgehalt den physiologischen Verhältnissen näher. Gefässwände sind für Wasser und kleinere Ionen frei durchlässig (Zellmembranen dagegen lassen nur Wasser frei durchtreten); Elektrolytlösungen verteilen sich deswegen im gesamten Extrazellulärraum, so dass üblicherweise nur rund ein Viertel ihres Volumens intravasal verbleibt.(1)
Kolloide
Als onkotisch wirksame Makromoleküle gebraucht man heute synthetisch produzierte Substanzen wie Dextran, Hydroxyäthylstärke oder Gelatine. Albuminlösungen werden zur Behandlung eines Volumenmangels nicht mehr empfohlen; sogar bei Hypoalbuminämie ist ihr Nutzen umstritten. Isoonkotische Lösungen, mit demselben kolloid- osmotischen Druck wie Plasma (3,3 kPa bzw. 25 mm Hg), sind eigentliche Plasmaersatzstoffe, während hyperonkotische als Plasmaexpander wirken, da ihr Volumeneffekt den der zugeführten Infusionsmenge übersteigt.
Kolloidale Lösungen enthalten jeweils eine Mischung von Makromolekülenunterschiedlicher Molekularmasse; um sie zu charakterisieren, gibt man eine mittlere Molekularmasse an. Am geläufigsten ist das «Gewichtsmittel» (Mw; bei Dextran 40 beträgt es z.B. 40’000 Dalton). Für die Wirkung und die Kinetik wichtiger ist jedoch das «Zahlenmittel » (Mn), die Summe aller Molekularmassen geteilt durch die Anzahl Moleküle.(2,3) Eine Übersicht zu den in der Schweiz erhältlichen künstlichen Kolloiden und ihren mittleren Molekularmassen liefert Tabelle 1.
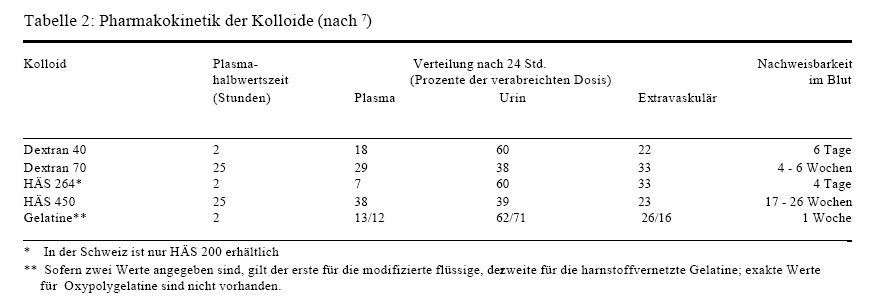
Die Nierenschwelle für Kolloide liegt bei einer Molekularmasse von etwa 50’000 D. Grössere Moleküle werden im Blut hydrolysiert oder im Gewebe gespeichert und dort abgebaut. Durch die Spaltung im Blut vermehren sich die onkotisch wirksamen Moleküle: so werden auch Moleküle nierengängig, die ursprünglich zu gross waren. Nähere pharmakokinetische Daten finden sich in Tabelle 2.
Alle Kolloide (inklusive Albumin) können anaphylaktoide Reaktionen -- von harmlosen Hautreaktionen bis zum Kreislauf- und Atemstillstand -- auslösen, wobei die zugrundeliegenden Mechanismen je nach Substanz verschieden sind. Um die Inzidenz der anaphylaktoiden Reaktionen zu erfassen, sind zahlreiche Untersuchungen durchgeführt worden. Weil aber die Ergebnisse abhängig von Aufbau und statistischer Auswertung der Studien stark differieren, kann man keine verbindlichen Zahlen nennen. Eine prospektive Multizenterstudie, welche die Daten von mehr als 200’000 Einzelinfusionen miteinbezog, liefert immerhin einen groben Hinweis auf die Grössenordnungen: Anaphylaktoide Reaktionen traten je nach verabreichtem Kolloid mit einer Häufigkeit von 1:1’000 bis 1:10’000 auf; die Raten der schweren Reaktionen betrugen 1:3’000 bis 1:30’000. Generell waren die anaphylaktoiden Reaktionen am häufigsten unter Gelatine, am seltensten unter Plasmaproteinen.(4)
Die Kolloide können die Blutgerinnung beeinflussen. Indem sie Wasser binden, werden die Gerinnungsfaktoren im Blut verdünnt. Dazu vermindert Dextran die Konzentration einer Faktor- VIII-Komponente, womit wahrscheinlich die Plättchenadhäsivität reduziert und die Auflösbarkeit von Thromben gesteigert wird.(5) Auch bei Hydroxyäthylstärke werden zusätzliche, spezifische Wirkungen auf das Gerinnungssystem diskutiert.(6) Bei Patienten mit Gerinnungsstörungen soll man Kolloide mit Vorsicht einsetzen, und allgemein sollten die Lösungen nicht in unbeschränkter Menge infundiert werden (für Dextran und Hydroxyäthylstärke gelten 20 ml/kg/Tag als obere Grenze). Kolloide können ins Gewebe übertreten und dort entweder gespeichert oder mit der Lymphe abtransportiert werden. In der Regel verändern gespeicherte Kolloide die Gewebsfunktionen nicht, auch wenn sich zuweilen Vakuolen mit darin vorhandenen Makromolekülen mikroskopisch nachweisen lassen.(7) Hydroxyäthylstärke kann anscheinend in seltenen Fällen zu einer Lebervergrösserung mit Aszites führen.(8)
Grössere Mengen von kolloidalen Lösungen (über 500 ml) können durch an der Erythrozytenoberfäche haftende Makromoleküle die Blutgruppenbestimmung verfälschen. (7)
Dextran
Dextran, ein wenig verzweigtes Glukosepolymer, wird mit Hilfe eines bakteriellen Enzyms aus Saccharose synthetisiert. Durch Hydrolyse entstehen Mischungen mit einer definierten mittleren Molekularmasse. In der Schweiz sind Dextran 40 und Dextran 70 erhältlich. Dextran 40 weist unter allen Kolloiden den stärksten initialen Volumeneffekt auf. Dextranlösungen besitzen noch zusätzliche Eigenschaften: Sie wirken thromboseprophylaktisch, und speziell Dextran 40 scheint durch eine Hemmung der Erythrozytenaggregation die Mikrozirkulation zu verbessern (was sich aber eventuell allein der starken Blutverdünnung zuschreiben lässt(3)).
Pharmakokinetik
Kleinere Dextranmoleküle werden über die Nieren, teilweise auch über den Darm ausgeschieden. Grössere werden von der Lymphe aufgenommen und in Geweben (nicht aber im Blut) durch das Enzym Dextranase abgebaut. Die renale Dextranclearance läuft ungefähr parallel mit der Kreatininclearance. Deshalb sollte die Dosis (vor allem von Dextran 40) bei Patienten mit stark eingeschränkter Nierenfunktion reduziert werden.(9)
Unerwünschte Wirkungen
Die dextranbedingten anaphylaktoiden Reaktionen werden vor allem durch antikörpervermittelte Immunkomplex- Reaktionen verursacht; bei den leichteren Reaktionen scheinen auch andere Mechanismen beteiligt zu sein. Da Dextran in Spuren in Nahrungsmitteln oder Zahnpasten vorhanden sein kann und Bestandteil von Streptokokken- Kapselpolysacchariden ist, findet man Antikörper bei einem namhaften Teil der Bevölkerung. Personen mit schweren anaphylaktoiden Reaktionen weisen oft sehr hohe Antikörper-Titer auf (vor allem IgG). Möglicherweise gibt es Leute, die -- genetisch determiniert -- durch Dextran stärker immunisiert werden und bei denen das Risiko einer schweren Allgemeinreaktion erhöht ist.(10,11) Unter höhermolekularen Dextranen ist das Risiko einer anaphylaktoiden Reaktion eventuell grösser als unter Dextran 40.(4) Es ist heute üblich, kurz vor der eigentlichen Dextraninfusion Dextran 1 (Promit®, monovalentes Dextran Fresenius ®) zu verabreichen. Dextran 1, mit einer mittleren Molekularmasse von 1’000 D, besteht aus ein paar wenigen Glukosemolekülen und wirkt als Hapten: ein Dextran- 1-Molekül vermag zwar eine Antikörper-Bindungsstelle zu besetzen, ist indessen zu klein, um zwischen mehreren Antikörpern Brücken und somit Immunkomplexe zu bilden. Leichte Reaktionen werden durch Dex-tran 1 kaum beeinflusst, weil Antikörper bei deren Entstehung offenbar eine geringere Rolle spielen. Bei mehreren zehntausend Patienten ist die Wirksamkeit von Dextran 1 geprüft worden. Dextran 1 senkt dosisabhängig das Risiko schwerer anaphylaktoider Reaktionen deutlich, hebt es jedoch nicht vollständig auf.(12,13) Seit Dextran 1 verwendet wird, hat in Schweden die Inzidenz schwerer anaphylaktoider Reaktionen nach Dextran von etwa 1:4’500 (pro Infusion) auf 1:84’000 abgenommen. In seltenen Fällen können auch nach Dextran 1 -- meistens mild verlaufende -- anaphylaktoide Reaktionen vorkommen.(14)
Eine hohe Dextrankonzentration macht den Urin viskös. Insbesondere Dextran 40 (von dem grosse Mengen rasch renal eliminiert werden) kann bei Patienten mit einem schweren Volumendefizit oder einer gestörten Nierenfunktion eine akute Niereninsuffizienz auslösen.(1)
Hydroxyäthylstärke
Hydroxyäthylstärke (HÄS) wird aus Amylopektin, einem Glukosepolymer und Hauptbestandteil der Stärke, gewonnen. Um den Abbau zu erschweren, sind an einzelne Glukosemoleküle Hydroxyäthylgruppen angehängt. Die Hydroxyäthylgruppen sind heterogen verteilt: fast die Hälfte aller Glukoseeinheiten enthält keine, der Rest 1 bis 3 Hydroxyäthylgruppen. Der Substitutionsgrad (durchschnittliche Zahl der Hydroxyäthylgruppen pro Glukosemolekül) ist neben der mittleren Molekularmasse die zweite Kenngrösse von Hydroxyäthylstärke.(15,16)
Pharmakokinetik
Moleküle, deren Grösse über der Nierenschwelle liegt, werden einerseits im Blut durch die a-Amylase zu 2 kleineren Molekülen gespalten, andererseits von Geweben aufgenommen und entweder vom RES abgebaut oder wieder ans Blut abgegeben. Die Hydrolyse läuft um so langsamer ab, je mehr Hydroxyäthylgruppen pro Glukoseeinheit vorhanden sind. Hydroxyäthylstärke-Moleküle können wochenlang im Körper verbleiben.(7,16)
Unerwünschte Wirkungen
Die Pathogenese der anaphylaktoiden Reaktionen ist noch offen; teilweise sind Antikörper sowie Veränderungen im Komplementsystem nachgewiesen worden.(11) Eine Prophylaxe ist nicht möglich. Hydroxyäthylstärke kann die a-Amylase- Konzentration im Serum, eventuell auch im Urin erhöhen. Der Blutzucker wird durch Hydroxyäthylstärke kaum beeinflusst, da die Moleküle ausgeschieden werden, bevor sie zu Glukose abgebaut worden sind.(16)
Die 10%ige HÄS-200-Lösung kann vermutlich wie Dextran 40 zu renalen Schädigungen führen.(3)
Gelatine
Gelatine (denaturiertes Kollagen) wird aus tierischen Knochen hergestellt. Nachdem die Polypeptidketten mehrmals gespalten worden sind, fügt man die Bruchstücke neu zusammen. Je nach Substanz, mit deren Hilfe die Ketten vernetzt werden, entstehen unterschiedliche Präparate: (1) modifizierte flüssige Gelatine (Physiogel ® SRK), (2) harnstoffvernetzte Gelatine (Haemaccel ® 35) oder (3) Oxypolygelatine (Gelifundol®). Ein relevanter Unterschied zwischen diesen 3 Produkten ist nicht bekannt.
Pharmakokinetik
Die Kinetik von Gelatinepräparaten ist wenig untersucht. Die Moleküle werden renal ausgeschieden; ob und allenfalls wie sie auch enzymatisch gespalten oder in Geweben gespeichert werden ist unklar.(7,9)
Unerwünschte Wirkungen
Auch bei Gelatine ist der genaue Mechanismus der anaphylaktoiden Reaktionen unbekannt. Vor allem bei der harnstoffvernetzten Gelatine vermutet man, dass sie zu einer Histaminfreisetzung führen kann. (Die heute erhältliche harnstoffvernetzte Gelatine soll dank eines höheren Reinigungsgrades weniger anaphylaktoide Reaktionen auslösen.) Eine Prä-medikation mit Histamin-H1- und H2-Rezeptorenblockern vermag die Inzidenz von anaphylaktoiden Reaktionen zu senken, hat sich aber in der klinischen Praxis nicht durchgesetzt.(3,11) Gelatine kann die Funktion von Fibronektin, einem Plasmaprotein, das die Phagozytose und Wundheilung unterstützt, beeinflussen. (17)
Klinische Studien
Die Wirksamkeit von Plasmaersatzstoffen wird am besten beurteilt, indem man bei hypovolämischen Patienten das Mass und die Dauer der Volumenexpansion misst; dies ist in kontrollierten Studien noch nicht genügend untersucht worden.(18) Meistens wurden neben den Kolloiden auch Blutkonserven und Elektrolytlösungen verabreicht, was Aussagen über die einzelnen Substanzen verunmöglicht. In einer Studie erhielten 83 Patienten im Laufe einer Wahloperation 1 l Infusionslösung mit einem Kolloid (Dextran 70, Hydroxyäthylstärke, harnstoffvernetzte Gelatine oder Albumin 5%) oder 0,9%ige Kochsalzlösung. Das Plasmavolumen nahm unter Dextran um durchschnittlich 790 ml, unter Hydroxyäthylstärke um 710 ml, unter Gelatine um 240 ml, unter Albumin um 490 ml und mit der Salzlösung um 180 ml zu.(19) Der initiale Effekt von Gelatine ist somit im Vergleich zu Dextran 70 oder Hydroxyäthylstärke deutlich geringer. Es ist aber denkbar, dass man Gelatinelösungen ohne Nachteile höher dosieren könnte, um dieselbe Wirkung wie mit anderen Kolloiden zu erzielen.
Immer wieder wird diskutiert, ob man zur Volumensubstitution Kristalloide oder Kolloide verwenden sollte. Der Kreislauf lässt sich mit Kristalloiden ebenso stabilisieren wie mit Kolloiden. Allerdings ist, verglichen mit Kolloiden, hiezu eine etwa zwei- bis viermal grössere Infusionsmenge notwendig. Deshalb ist zumindest theoretisch bei Kristalloiden die Gefahr einer Volumenüberladung (Lungenödem usw.) grösser als bei Kolloiden.(1) In einer kürzlich veröffentlichten Meta-Analyse wurden 8 Studien zusammengefasst, welche die Mortalität nach der Infusion von Kolloiden bzw. Kristalloiden angegeben hatten. Bei Patienten, die ein Trauma erlitten hatten, war die Mortalität unter kristalloiden Lösungen geringer, bei den übrigen diejenige unter kolloidalen. Alle Daten zusammengenommen, ergab sich für Kristalloide ein leicht besseres Resultat.(20) Für einen Grossteil der Patienten ist es wahrscheinlich unerheblich, ob sie zur Volumensubstitution Kristalloide oder Kolloide erhalten. Es wäre die Aufgabe künftiger Untersuchungen, herauszufinden, bei welchen Untergruppen von Patienten die Wahl der Infusionslösung wirklich eine Rolle spielt.(21) Ein neues Konzept, das die Infusion kleiner Volumina propagiert, kombiniert Kristalloide und Kolloide fix: Bereits 250 ml einer hypertonenhyperonkotischen Lösung (Dextran 70 in 7,5%iger NaCl- Lösung) scheinen zu genügen, um die Kreislauffunktion primär aufrechtzuerhalten.(22)
Schlussfolgerungen
Eine Volumensubstitution kann man mit kristalloiden oder mit kolloidalen Lösungen durchführen; ein klinisch relevanter Unterschied ist bislang nicht dokumentiert. Aufgrund theoretischer Überlegungen wird man aber bei Patienten, die durch eine zu grosse Flüssigkeitsmenge gefährdet sind, Kolloide -- im allgemeinen zusammen mit Elektrolytlösungen -- verabreichen.
Auch wenn die einzelnen Kolloide z.T. als nicht ebenbürtig eingestuft werden, lässt sich nicht umfassend beantworten, welche Substanz zu bevorzugen sei. Dextran 70 eignet sich zur Volumensubstitution wohl eher als Dextran 40, welches das Plasmavolumen oft fast zu stark expandiert und bei dem das Risiko renaler Nebenwirkungen höher ist (dasselbe gilt wahrscheinlich auch für die 10%ige HÄS- 200-Lösung).
Man soll die spezifischen Eigenschaften der Kolloide kennen und sie demgemäss einsetzen. Es ist weitaus wichtiger, dass man einen Volumenmangel behandelt als womit man ihn behandelt.
Literatur
- 1) Falk JL et al. Acute Care 1984; 10: 59-94
- 2) Gruber UF. Blood Replacement. Berlin: Springer, 1969: 53
- 3) Lundsgaard-Hansen P. Anästhesiol Reanim 1984; 9: 3-18
- 4) Ring J, Messmer K. Lancet 1977; 1: 466-9
- 5) Bergqvist D. Acta Chir Scand 1982; 148: 633-40
- 6) Strauss RG. Transfusion 1981; 21: 299-302
- 7) Mishler JM. Clin Haematol 1984; 13: 75-92
- 8) Pfeifer U et al. Klin Wochenschr 1984; 62: 862-6
- 9) Klotz U, Kroemer H. Clin Pharmacokinet 1987; 12: 123-35
- 10) Hedin H et al. Dev Biol Stand 1981; 48: 179-89
- 11) Ring J. Clin Anaesthesiol 1984; 2: 619-41
- 12) Ljungström KG et al. Acta Chir Scand 1983; 149: 341-8
- 13) Renck H et al. Acta Chir Scand 1983; 149: 355-60
- 14) Ljungström KG et al. Anaesthesia 1988; 43: 729-32
- 15) Thompson WL. Dev Biol Stand 1981; 48: 259-66
- 16) Hulse JD, Yacobi A. Drug Intell Clin Pharm 1983; 17: 334-41
- 17) Brodin B et al. Scand J Clin Lab Invest 1984; 44: 529-33
- 18) Drug Ther Bull 1987; 25: 37-9
- 19) Lamke LO, Liljedahl SO. Resuscitation 1976; 5: 93-102
- 20) Velanovich V. Surgery 1989; 105: 65-71
- 21) Fisher MM. Theor Surg 1989; 4: 205-11
- 22) Holcroft JW et al. Ann Surg 1987; 206: 279-87
Standpunkte und Meinungen
- Es gibt zu diesem Artikel keine Leserkommentare.
Copyright © 2024 Infomed-Verlags-AG
PK579
Gratisbuch bei einem Neuabo!
pharma-kritik abonnieren
-
Jahrgang 45 / 2023
Jahrgang 44 / 2022
Jahrgang 43 / 2021
Jahrgang 42 / 2020
Jahrgang 41 / 2019
Jahrgang 40 / 2018
Jahrgang 39 / 2017
Jahrgang 38 / 2016
Jahrgang 37 / 2015
Jahrgang 36 / 2014
Jahrgang 35 / 2013
Jahrgang 34 / 2012
Jahrgang 33 / 2011
Jahrgang 32 / 2010
Jahrgang 31 / 2009
Jahrgang 30 / 2008
Jahrgang 29 / 2007
Jahrgang 28 / 2006
Jahrgang 27 / 2005
Jahrgang 26 / 2004
Jahrgang 25 / 2003
Jahrgang 24 / 2002
Jahrgang 23 / 2001
Jahrgang 22 / 2000
Jahrgang 21 / 1999
Jahrgang 20 / 1998
Jahrgang 19 / 1997
Jahrgang 18 / 1996
Jahrgang 17 / 1995
Jahrgang 16 / 1994
Jahrgang 15 / 1993
Jahrgang 14 / 1992
Jahrgang 13 / 1991
Jahrgang 12 / 1990
Jahrgang 11 / 1989
Jahrgang 10 / 1988
Kennen Sie "100 wichtige Medikamente" schon?
Die Liste der 100 Medikamente sehen Sie auf der Startseite von 100 Medikamente.