Parkinson-Therapie heute
- Autor(en): Hans-Peter Ludin
- pharma-kritik-Jahrgang 33
, Nummer 8/9, PK864
Redaktionsschluss: 2. März 2012
DOI: https://doi.org/10.37667/pk.2011.864 - PDF-Download der Printversion dieser pharma-kritik Nummer
Seit der ersten erfolgreichen Anwendung von Levodopa (L-Dopa) sind jetzt mehr als 50 Jahre vergangen.(1) Inzwischen sind zahlreiche weitere Behandlungsmöglichkeiten verfügbar geworden. Bis heute ist L-Dopa in Kombination mit einem Dekarboxylasehemmer (DH) der Goldstandard geblieben. An diesem werden alle anderen Therapien gemessen. Alle unsere Behandlungen sind weiterhin symptomatisch, eine kausale Therapie ist nicht in Sicht. Trotz zahlreicher diesbezüglicher Versuche blieben mögliche neuroprotektive Massnahmen bisher unbewiesen.
In den letzten Jahren hat sich unser Konzept der Krankheit stark verändert. Während langer Zeit wurde der Morbus Parkinson als praktisch rein motorisches Krankheitsbild gesehen, verursacht durch den Untergang dopaminerger Neuronen in der Substantia nigra. Inzwischen ist aber klar geworden, dass zahlreiche nicht-motorische Symptome, die grösstenteils nicht auf den Dopaminmangel zurückzuführen und durch die Beteiligung anderer Hirnareale bedingt sind, dazukommen und besonders in den späteren Krankheitsstadien das Bild sogar beherrschen.(2) Vielfach gehen psychische, vegetative und sensorische Symptome der motorischen Symptomatik in Form von Depressionen, Obstipation, REM-Schlafverhaltensstörung und Abnahme des Riechvermögens zeitlich deutlich voraus. Sie sind allerdings zu wenig spezifisch, als dass daraus diagnostische Schlüsse gezogen werden könnten. Ein zuverlässiger Marker für diese prämotorische Phase ist vorerst nicht verfügbar.
Fakten zu den Medikamenten
L-Dopa (Levodopa)
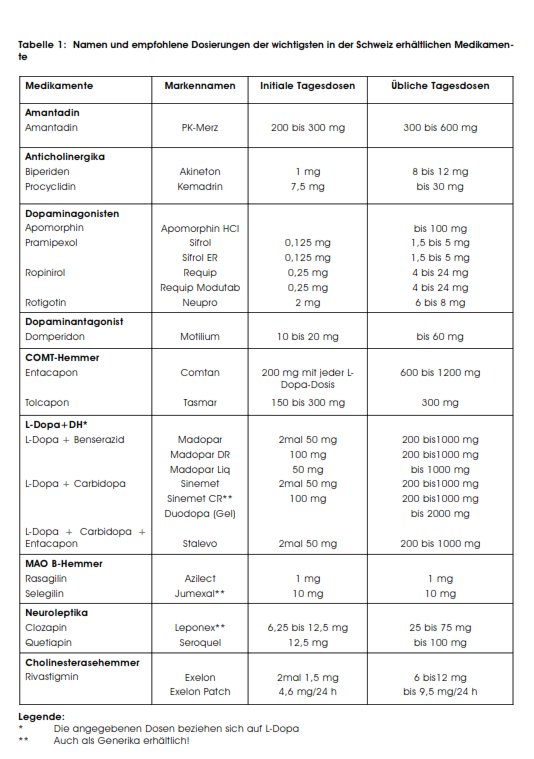
L-Dopa ist der chemische Vorläufer von Dopamin. Dieses kann die Blut-Hirnschranke nicht durchdringen. Zur Substitution des zerebralen Dopaminmangels wird deshalb L-Dopa eingesetzt. Da L-Dopa in der Peripherie zum grössten Teil zu Dopamin dekarboxyliert wird, wird es immer mit einem peripheren Dekarboxylase-Hemmer (DH, Benserazid oder Carbidopa) kombiniert. Die entsprechenden Markennamen sind in der Tabelle 1 zu finden.
Da L-Dopa zusätzlich durch die Catechol-O-Methyl-Transferase (COMT) zu 3-O-Methyl-Dopa methyliert wird, kann dieser Umbau in besonderen Situationen durch einen COMT-Hemmer (Entacapon oder Tolcapon) weitgehend blockiert werden.
Da L-Dopa+DH eine Halbwertszeit von weniger als 2 Stunden hat, wurde eine Verlängerung der Wirkungsdauer der Einzeldosen durch Retard-Präparate angestrebt. Die Zahl der täglich benötigten Dosen kann damit aber nur marginal reduziert werden. Ausserdem haben diese Präparate eine deutlich reduzierte Bioverfügbarkeit und die Resorption ist häufig erratisch.
Am Beginn der Behandlung können Übelkeit und Erbrechen auftreten, die mit Domperidon bekämpft werden können. In den meisten Fällen treten mit der Zeit mehr oder weniger ausgeprägte Fluktuationen und unwillkürliche Bewegungen auf. Viele Behandelte berichten über vermehrte und lebhaftere Träume. Besonders, aber nicht ausschliesslich bei Personen mit kognitiven Defiziten kann es zu Verwirrtheit und Halluzinationen kommen. Zu einer Impuls-Kontrollstörung kommt es unter L-Dopa seltener als unter Dopaminagonisten.
COMT-Hemmer (Catechol-O-Methyl-Transferase-Hemmer)
Die COMT-Hemmer verhindern die Umwandlung von L-Dopa in 3-O-Methyldopa. Damit kommt mehr L-Dopa ins Gehirn, wo es zu Dopamin dekarboxyliert werden kann. Die Gabe eines COMT-Hemmers ist daher nur zusammen mit L-Dopa+DH wirksam.
Auf dem Markt sind die beiden COMT-Hemmer Entacapon und Tolcapon. Tolcapon ist eindeutig wirksamer als Entacapon. Da Tolcapon ein erhebliches hepatotoxisches Potential aufweist, sind regelmässige Kontrollen der Leberwerte erforderlich.
Entacapon hat ungefähr die gleiche Halbwertszeit wie L-Dopa+DH und muss daher zusammen mit jeder Dosis eingenommen werden. Tolcapon hat eine längere Halbwertszeit, so dass 3 tägliche Dosen genügen.
Dopaminagonisten
Seit den 70-er Jahren des 20. Jahrhunderts werden Dopaminagonisten in der Behandlung des Parkinsonsyndroms eingesetzt. Nach Bromocriptin (Parlodel®) kamen verschiedene ergoline und nicht-ergoline Substanzen auf den Markt. Seit bekannt wurde, dass besonders unter Pergolid gehäuft valvuläre Fibrosen auftreten,(3) werden praktisch nur noch die nicht-ergolinen Substanzen Pramipexol, Ropinirol und Rotigotin eingesetzt. Von Pramipexol und Ropinirol existieren Retardpräparate. Rotigotin wird als Hautpflaster verwendet.(4)
Die Dopaminagonisten weisen eine geringere maximale Wirkung auf als L-Dopa. In frühen Krankheitsstadien kann damit die Symptomatik aber meistens befriedigend kontrolliert werden. Als frühe Nebenwirkungen müssen auch hier Übelkeit und Erbrechen erwähnt werden. Psychische Nebenwirkungen, besonders die Impulskontrollstörungen, sind häufiger als unter L-Dopa+DH. Häufig kommt es auch zur Sedation, gefürchtet sind die plötzlichen Schlafattacken.(5) Es kann zu peripheren Ödemen kommen. Das Rotigotin-Hautpflaster kann Hautreaktionen an der Applikationsstelle verursachen.
Eine Sonderstellung unter Dopaminagonisten nimmt Apomorphin ein. Apomorphin hat eine kurze Halbwertszeit von 30-60 min und ausserdem wirkt es bei oraler Gabe in wirksamen Dosen nephrotoxisch. Es wird deshalb praktisch ausschliesslich in fortgeschrittenen Krankheitsstadien als Lösung subkutan injiziert. Neben den erwähnten Nebenwirkungen der Dopaminagonisten sind die häufigen Hautreaktionen an den Injektionsstellen und die seltenen hämolytischen Anämien zu beachten.
Anticholinergika
Anticholinergika sind die ältesten Medikamente, die in der Behandlung des Parkinsonsyndroms eingesetzt werden. Sie wirken fast ausschliesslich auf den Tremor.
Neben den bekannten peripheren Nebenwirkungen (Mundtrockenheit, Störungen der Akkomodation, der Magenentleerung und der Miktion usw.) sind besonders die möglichen psychischen Wirkungen, die bis zur Pseudodemenz und zum Delir gehen können, zu beachten. Besonders bei älteren Kranken sollten sie deshalb nur mit grösster Vorsicht gegeben werden.
Amantadin
Amantadin, ein Antagonist von N-Methyl-D-Aspartat (NMDA), hat eine geringe Anti-Parkinson-Wirkung, die in den meisten Fällen nach wenigen Monaten praktisch verschwindet. Die wichtigste Indikation für Amantadin ist heute seine antidyskinetische Wirkung. Als intravenös injizierbare Lösung kann es in besonderen Situationen (akinetische Krise, postoperativ) eingesetzt werden.
MAO-B-Hemmer
Dopamin wird im Gehirn einerseits durch eine MAO B zu Dihydroxyphenyl-Essigsäure (DOPAC) und anderseits durch die COMT zu 3-Methoxytyramin (3-MT) oxidiert. Diese Zwischenprodukte werden ihrerseits durch die COMT und die MAO B zu Homovanillinsäure abgebaut. Die irreversiblen MAO-B-Hemmer Rasagilin und Selegilin verstärken und verlängern die Wirkung von Dopamin. Beide Substanzen haben eine moderate, aber eindeutige Wirkung auf die Parkinsonsymptomatik.(6)
MAO-B-Hemmer dürfen nicht mit einem MAO-A-Hemmer kombiniert werden. Auch sollten sie nicht zusammen mit Tolcapon gegeben werden. Dieses hat neben der peripheren auch eine zentrale Wirkung, so dass es zusammen mit einem MAO-B-Hemmer zu einer Akkumulation von Dopamin kommen könnte, das nicht mehr oder nicht genügend abgebaut werden kann.
Eine vermutete neuroprotektive Wirkung von Rasagilin konnte bisher weder eindeutig bewiesen noch widerlegt werden.(7)
MAO-B-Hemmer können zu Nausea und orthostatischer Hypotonie führen. Diätetische Massnahmen, insbesondere die Vermeidung von tyraminreichen Nahrungsmitteln, erübrigen sich.
Empfehlungen
Die folgenden Empfehlungen richten sich weitgehend nach den Richtlinien der Therapiekommission der Schweizerischen Neurologischen Gesellschaft aus dem Jahre 2008.(8) Die Namen und die empfohlenen Dosierungen der wichtigsten Medikamente sind in Tabelle 1 aufgelistet.
Wann und wie soll mit der medikamentösen Behandlung begonnen werden?
Solange wir über keine kausale Behandlung verfügen, drängt sich ein möglichst früher Therapiebeginn nicht auf. Während längerer Zeit wurde sogar empfohlen, den Therapiebeginn hinauszuschieben, um motorische Komplikationen der Therapie (Fluktuationen, Dyskinesien und Dystonien) möglichst lange zu vermeiden. Inzwischen herrscht aber die Meinung vor, dass sich dieses Vorgehen aus den folgenden Gründen nicht lohnt: Das Auftreten dieser Komplikationen hängt nicht nur von der Behandlungsdauer, sondern auch von Stadium der Krankheit ab. Bei einem späteren Therapiebeginn treten sie umso früher auf. Ausserdem wird mit dem Zuwarten die Phase mit den besten Therapieergebnissen («honeymoon-Phase») verpasst. Im Weiteren gibt es Hinweise darauf, dass es Kranken mit frühem Therapiebeginn gegenüber solchen mit späterem Beginn auch später besser geht.(9) Die Therapie sollte deshalb gestartet werden, wenn sich die Patientin oder der Patient im Alltag beeinträchtigt fühlt und der entsprechende Leidensdruck vorliegt.
Beim Vorliegen einer Tremor-dominanten Symptomatik wird die medikamentöse Behandlung manchmal mit einem Anticholinergikum begonnen. Besonders bei älteren Kranken ist aber dabei besonders wegen der möglichen psychischen Nebenwirkungen grosse Vorsicht geboten. Die Dosierung muss langsam gesteigert werden und die Behandelten und ihre Angehörigen müssen auf mögliche Denkstörungen und Verwirrtheit aufmerksam gemacht werden.
Bei jüngeren Kranken (<65-70 Jahre) ohne kognitive Störungen wird die Behandlung in der Regel mit einem nicht-ergolinen Dopaminagonisten (Pramipexol, Ropinirol, Rotigotin, Markennamen siehe Tabelle 1) begonnen. Es konnte gezeigt werden, dass unter Dopaminagonisten weniger motorische Komplikationen der Therapie auftreten als unter L-Dopa.(10,11) Auch hier muss die Dosis schrittweise erhöht werden. Sollten anfänglich Nausea oder Erbrechen auftreten, kann vorübergehend Domperidon dazugegeben werden. Die Dopaminagonisten weisen eine geringere maximale Wirkung auf als L-Dopa+DH. Früher oder später muss die L-Dopa-DH-Kombination bei praktisch allen Kranken dazugegeben werden.
Bei älteren Personen und bei solchen mit kognitiven Defiziten wird die Therapie mit L-Dopa+DH gestartet. Damit ist das Risiko psychischer Nebenwirkungen kleiner als mit den Dopaminagonisten. Da L-Dopa mit dem Essen zusammen nicht zuverlässig resorbiert wird, soll das Präparat eine halbe bis eine Stunde vor dem Essen (oder allenfalls zwei Stunden nachher) eingenommen werden.
Es wurde vermutet, dass die Zugabe eines Hemmers der Catechol-O-Methyltransferase (COMT) vom Beginn der Behandlung mit L-Dopa+DH an zu einer Verzögerung des Auftretens von motorischen Komplikationen führen könnte. Diese Annahme konnte aber nicht bestätigt werden. Dyskinesien traten mit COMT-Hemmer sogar früher auf als ohne.(12) Wird ein COMT-Hemmer hinzugefügt, muss deshalb die Dosis von L-Dopa+DH reduziert werden.
Behandlung der motorischen Komplikationen der dopaminergen Therapie
Nach der bereits erwähnten Honeymoon-Phase, die einige Monate bis mehrere Jahre dauern kann, kommt es bei vielen Behandelten zu Wirkungsschwankungen (Fluktuationen), die sich zuerst in einer verkürzten Wirkung der Einzeldosen («wearing-off») äussern. Gegen das Ende der Wirkungsdauer kommt es zu einer Zunahme oder zum Wiederauftreten der Kardinalsymptome Akinese, Rigor und Tremor. Diese Phasen werden von den Betroffenen als sehr unangenehm empfunden, da sie meist von psychischen und vegetativen Symptomen begleitet werden. Später zeigen diese Fluktuationen keine eindeutige Abhängigkeit von der Einnahme der Medikamente mehr («on-off-Phänomen»).
Meistens bringt der Einsatz von Retardpräparaten von L-Dopa+DH keine überzeugende Besserung. Gute Resultate können hingegen mit den COMT-Hemmern Entacapon und Tolcapon erzielt werden.(13) Es kann auch versucht werden, durch die Kombination mit einem Dopaminagonisten oder einem MAO-B-Hemmer eine konstantere Wirkung zu erzielen. Mit der Zeit wird es aber häufig unumgänglich, die tägliche Dosis in kleinere und häufigere Einzeldosen zu fraktionieren.
Besonders in den «on»-Phasen treten mit der Zeit unwillkürliche choreatische Bewegungen (Dyskinesien) auf. Häufig werden sie von den Kranken selbst gar nicht wahrgenommen. Sie können so schwach sein, dass sie nur von Erfahrenen sicher erkannt werden. Nicht selten werden sie auch in «Pseudowillkür-Bewegungen» eingebaut. Sie können aber auch sehr heftig werden, so dass sie für die Betroffenen eine grosse Anstrengung bedeuten, mit Willkürbewegungen stark interferieren und auch zu Gleichgewichtsproblemen führen.
Als Behandlungsmöglichkeiten bieten sich hier ebenfalls das Fraktionieren der Einzeldosen, vermehrte Gabe von Dopaminagonisten zu Ungunsten von L-Dopa+DH und die Zugabe von Amantadin an.(14) Bei ungenügender Wirkung von Amantadin oder beim Auftreten von bedeutsamen Nebenwirkungen (z.B. kognitive Störungen), kann Clozapin eine Besserung bringen.
Dystone Krämpfe, die sehr schmerzhaft sein können, treten vor allem beim Abfluten der dopaminergen Medikation auf. Besonders häufig sind sie nachts und in den frühen Morgenstunden. Manchmal sind deshalb zusätzliche nächtliche Medikamentendosen nötig. Die Krämpfe sprechen am schnellsten auf wasserlösliche Präparate von L-Dopa+DH oder auf einzelne subkutane Apomorphin-Boli an. Bei anhaltenden Dystonien können mit Injektionen von Botulinumtoxin gute Resultate erzielt werden.(15) Leider können die motorischen Komplikationen mit zunehmender Krankheitsdauer immer häufiger werden, so dass mit den beschriebenen Massnahmen kein einigermassen befriedigendes Resultat mehr erzielt werden kann. In diesen Fällen bieten sich heute invasivere Methoden an, die bei sorgfältiger Selektion gute Resultate versprechen. In Frage kommt die tiefe Hirnstimulation(16) oder die extrakorporalen Pumpentherapien mit subkutanem Apomorphin(17) oder mit einem L-Dopa+Carbidopa-Gel,(18,19) der über eine PEG-Sonde direkt ins proximale Jejunum abgegeben wird. Alle diese Behandlungen können nur unter stationären Bedingungen initiiert werden. Der Entscheid, welche dieser Behandlungen individuell am besten geeignet ist, muss aufgrund verschiedener Kriterien, die in Tabelle 2 skizziert werden, und den Präferenzen der Betroffenen gefällt werden.
Behandlung der psychischen Nebenwirkungen
In späteren Krankheitsstadien, besonders wenn schon kognitive Defizite vorliegen, kommt es zu Verwirrtheit, illusionären Verkennungen und Halluzinationen. Vorboten davon sind häufig unruhiger Schlaf und vermehrte Träume, die bis zu Horrorträumen gehen können. Die Halluzinationen sind fast immer rein optisch. Meistens haben die Betroffenen eine deutliche Distanz zu den Wahnvorstellungen und manchmal realisieren sie auch, dass es sich um solche handelt. Falls diese Erscheinungen schon in frühen Krankheitsstadien und allenfalls sogar vor dem Beginn der dopaminergen Therapie auftreten, muss differentialdiagnostisch an die diffuse Lewy-Körperchen-Krankheit gedacht werden.
Beim Auftreten der beschriebenen Nebenwirkungen müssen Anticholinergika, aber auch MAO-B-Hemmer und Amantadin abgesetzt werden. Häufig lohnt es sich auch, die Tagesdosen der Dopaminagonisten zugunsten von L-Dopa+DH zu reduzieren. Die Empfehlung, die letzte Dosis der Medikamente auf 16 bis 17 Uhr vorzuverschieben, ist meistens nicht realisierbar, weil die nächtliche Akinese sonst unerträglich wird.
Vielfach wird der Einsatz eines Neuroleptikums unumgänglich. Parkinsonkranken dürfen nur Quetiapin oder Clozapin verschrieben werden. Alle anderen Neuroleptika führen zu einer Zunahme der motorischen Symptomatik.(20) Clozapin ist eindeutig potenter als Quetiapin; wegen des Risikos einer Agranulozytose sind aber regelmässige Blutbildkontrollen unerlässlich. Parkinsonkranke benötigen und vertragen meist nur relativ kleine Dosen dieser Medikamente. Es empfiehlt sich, die Dosierung einzuschleichen. Eine Dosis von 50 mg Clozapin pro Tag ist selten notwendig.
Tritt ein depressives Syndrom auf, so ist eine antidepressive Therapie, z.B. mit einem Serotonin-Wiederaufnahmehemmer (SSRI), indiziert. Der Dopaminagonist Pramipexol hat auch eine gewisse antidepressive Wirkung.
Die dopaminergische Therapie kann zu einer Impulskontrollstörung und dem Dopamin-Dysregulations-Syndrom (DDS) führen. Dieser Problematik wurde lange zu wenig Beachtung geschenkt.(21,22) Dies liegt zum Teil daran, dass die entsprechenden Symptome in der Sprechstunde meistens nicht spontan erwähnt werden. Deshalb muss aktiv danach gefragt werden. Es wird geschätzt, dass bei bis zu 17% der Kranken entsprechende Symptome vorliegen, wobei jüngere Männer am häufigsten betroffen sind. Das Syndrom hat verschiedene Facetten, am häufigsten sind Impulskontrollstörungen mit Hypersexualität, pathologischer Spielsucht, pathologischem Einkaufen oder Störungen des Essverhaltens. Besonders die Hypersexualität (oft verbunden mit einer erektilen Dysfunktion) kann zu Problemen in der Partnerschaft und zu finanziellen Schwierigkeiten (Bordellbesuche, Telefonsex usw.) führen. Daneben kann es zu einer Abhängigkeit von den Dopaminergika führen, deren Dosen ohne motorischen Gewinn immer weiter gesteigert werden. Die Stimmung kann zwischen unangepasster Euphorie und Suizidalität schwanken. Im Rahmen des DDS kann es auch zu stereotypen motorischen Handlungen («Punding») kommen.
Da die erwähnten Störungen häufiger durch Dopaminagonisten als durch L-Dopa+DH bedingt sind, lohnt es sich, zuerst erstere zu reduzieren oder abzusetzen. Wenn jemand von den Medikamenten abhängig oder suizidal ist, gelingt der Entzug meist nur unter stationären Bedingungen. Vielfach ist zumindest vorübergehend eine zusätzliche Therapie mit Quetiapin oder Clozapin nötig.
Nicht-medikamentöse Therapie
Zur Optimierung des Bewegungsablaufs tragen neben den Medikamenten auch physiotherapeutische sowie eventuell ergotherapeutische Massnahmen bei.
Behandlung der nicht-motorischen Störungen
Es ist nicht möglich, im Rahmen dieser Übersicht auf die Therapie der nicht-motorischen Störungen im Einzelnen einzugehen. Eine Zusammenfassung des Wissensstands findet sich in einer neueren Übersicht.(23) Hier sei lediglich auf das Problem der dementiellen Entwicklung hingewiesen. Parkinsonkranke haben in fortgeschrittenen Stadien ein etwa fünfmal grösseres Risiko einer Demenz als die Durchschnittsbevölkerung. Es konnte gezeigt werden, dass bei der Parkinsondemenz mit dem zentral wirkenden Cholinesterasehemmer Rivastigmin eine statistisch signifikante Besserung erzielt werden kann, ohne gleichzeitig die Parkinsonsymptomatik negativ zu beeinflussen.(24) Klinisch sind die zu beobachtenden Effekte nicht immer überzeugend, so dass sich die länger dauernde Verwendung nur bei Personen lohnt, die gut auf die Behandlung ansprechen. Rivastigmin kann aber auch zur Behandlung von Halluzinationen eingesetzt werden, wodurch manchmal die Verabreichung von Neuroleptika (Clozapin, Quetiapin) vermieden werden kann.
Literatur
- 1) Birkmayer W, Hornykiewicz O. Wien Klin Wschr 1961; 73: 787-8
- 2) Braak H et al. Mov Disord 2006; 21: 2041-51
- 3) Zanettini R et al. N Engl J Med 2007; 356: 39-46
- 4) Parkinson Study Group. Arch Neurol 2003; 60: 1721-8
- 5) Frucht S et al. Neurology 1999; 52: 1908-10
- 6) Parkinson Study Group. Arch Neurol 2004; 61: 561-6
- 7) Olanow CW et al. N Engl J Med 2009; 361: 1268-78
- 8) Arbeitsgruppe der Therapiekommission der Schweizerischen Neuro- logischen Gesellschaft (SNG). Schweiz Arch Neurol Psychiat 2008;159: 429-35
- 9) Fahn S et al. N Engl J Med 2004; 351: 2498-508
- 10) Holloway RG et al. Arch Neurol 2004; 61: 1044-53
- 11) Rascol O et al. Mov Disord 2006; 21: 1844-50
- 12) Stocchi F et al. Ann Neurol 2010; 68:18-27
- 13) Dewey RB Jr. Neurology 2004; 62 (Suppl 4), S3-7
- 14) Wolf E et al. Mov Disord 2010; 25: 1357-63
- 15) Pacchetti C et al. Mov Disord 1995; 10: 333-6
- 16) Deuschl G et al. N Engl J Med 2006; 355: 896-908
- 17) Katzenschlager R et al. Mov Disord 2005; 20: 151-7
- 18) Nyholm D et al. Neurology 2005; 64: 216-23
- 19) Lisitchkina H et al. Schweiz Arch Neurol Psychiat 2011; 162: 122-6
- 20) Richard IH, Nutt J. Neurology 2000; 55: 748-9
- 21) Evans AH et al. Mov Disord 2009; 24: 1561-70
- 22) Weintraub D et al. Arch Neurol 2010 ; 67: 589-95
- 23) Zesiewicz TA et al. Neurology 2010; 74: 924-31
- 24) Emre M et al. N Engl J Med 2004; 351: 2509-18
Standpunkte und Meinungen
- Es gibt zu diesem Artikel keine Leserkommentare.
Copyright © 2024 Infomed-Verlags-AG
PK864
Verwandte Artikel
LoginGratisbuch bei einem Neuabo!
pharma-kritik abonnieren
-
Jahrgang 45 / 2023
Jahrgang 44 / 2022
Jahrgang 43 / 2021
Jahrgang 42 / 2020
Jahrgang 41 / 2019
Jahrgang 40 / 2018
Jahrgang 39 / 2017
Jahrgang 38 / 2016
Jahrgang 37 / 2015
Jahrgang 36 / 2014
Jahrgang 35 / 2013
Jahrgang 34 / 2012
Jahrgang 33 / 2011
Jahrgang 32 / 2010
Jahrgang 31 / 2009
Jahrgang 30 / 2008
Jahrgang 29 / 2007
Jahrgang 28 / 2006
Jahrgang 27 / 2005
Jahrgang 26 / 2004
Jahrgang 25 / 2003
Jahrgang 24 / 2002
Jahrgang 23 / 2001
Jahrgang 22 / 2000
Jahrgang 21 / 1999
Jahrgang 20 / 1998
Jahrgang 19 / 1997
Jahrgang 18 / 1996
Jahrgang 17 / 1995
Jahrgang 16 / 1994
Jahrgang 15 / 1993
Jahrgang 14 / 1992
Jahrgang 13 / 1991
Jahrgang 12 / 1990
Jahrgang 11 / 1989
Jahrgang 10 / 1988
Kennen Sie "100 wichtige Medikamente" schon?
Die Liste der 100 Medikamente sehen Sie auf der Startseite von 100 Medikamente.